Фармакодинамика
Механизм действия
Деносумаб представляет собой человеческое моноклональное антитело (IgG2), обладающее высокой аффинностью и специфичностью к лиганду рецептора активатора ядерного фактора каппа В (RANKL) и тем самым препятствует активации рецептора RANK, расположенного на поверхности остеокластов и их предшественников. Предотвращение взаимодействия RANKL/RANK ингибирует образование, активацию и выживаемость остеокластов, приводя к уменьшению костной резорбции в кортикальных и трабекулярных слоях кости.
Фармакодинамические эффекты
Лечение препаратом Пролиа® приводило к быстрому снижению скорости ремоделирования кости, достигая минимальных (снижение на 85%) сывороточных концентраций маркера костной резорбции – 1С-телопептида (СТХ) в течение 3 дней. Уменьшение концентрации СТХ оставалось стабильным в интервале между введениями препарата. В конце каждого интервала дозирования выраженность снижения концентрации СТХ в сыворотке крови частично уменьшалась от максимального снижения ≥ 87% до приблизительно ≥ 45% (диапазон 45-80%), что отражает обратимость влияния Пролиа® на ремоделирование кости при снижении концентрации деносумаба в сыворотке крови. Данные эффекты наблюдались на протяжении всего курса лечения. Маркеры ремоделирования кости, как правило, достигали концентраций периода до начала лечения не позднее, чем через 9 месяцев после введения последней дозы препарата. После возобновления лечения деносумабом степень снижения концентраций СТХ была сходна со степенью снижения концентрации СТХ в начале курса лечения деносумабом.
Иммуногенность
По данным клинических исследований во время применения деносумаба не наблюдалось образования нейтрализующих антител. С помощью метода чувствительного иммуноанализа было показано, что менее чем у 1 % пациентов, получавших деносумаб в течение периода времени до 5 лет, определялись не нейтрализующие связывающие антитела без признаков влияния на фармакокинетический профиль, токсичность или клинический ответ.
Клиническая эффективность и безопасность у женщин в постменопаузе с остеопорозом
Эффективность и безопасность Пролиа®, вводимого каждые 6 месяцев в течение трех лет, исследовались на женщинах с постменопаузальным остеопорозом ( 7808 женщин в возрасте 60-91 год, из которых у 23,6% отмечались часто встречающиеся переломы позвонков) с исходной минеральной плотностью костей (Т-критерий) в поясничном отделе позвоночника или бедре между -2,5 и -4,0 и средней абсолютной 10-летней вероятностью возникновения переломов 18,60% (децили: 7,9-32,4%) для крупных остеопоротических переломов и 7,22% (децили: 1,4-14,9%) для переломов бедра. Женщины с другими заболеваниями или находящиеся на терапии, которая может оказывать влияние на кости, были исключены из исследования. Дополнительно женщины ежедневно получали кальций (не менее 1 000 мг) и витамин D (не менее 400 МЕ).
Влияние на вертебральные переломы
Пролиа® значительно снижает риск появления новых вертебральных переломов через 1, 2 и 3 года после начала терапии (р < 0,0001) (смотрите таблицу 1 ниже).
Таблица 1 Влияние Пролиа® на риск новых вертебральных переломов
|
|
Количественное соотношение женщин с переломами (%)
|
Снижение
абсолютного риска (%)
(95% CI)
|
Снижение
относительного риска (%)
(95% CI)
|
|
|
Плацебо
n=3906
|
Пролиа® n=3902
|
|
0-1 год
|
2,2
|
0,9
|
1,4 (0,8, 1,9)
|
61 (42, 74)**
|
|
0-2 года
|
5,0
|
1,4
|
3,5 (2,7, 4,3)
|
71 (61 79)**
|
|
0-3 года
|
7,2
|
2,3
|
4,8 (3,9, 5,8)
|
68 (59,74)*
|
*р < 0,0001, **р < 0,0001 — исследовательский анализ
Влияние на перелом бедра
Пролиа® показала 40% относительное снижение (0,5% снижение абсолютного риска) риска перелома бедра в течение трех лет (p < 0,05). Частота перелома бедра составила 1,2% в группе плацебо по сравнению с 0,7% в группе приема Пролиа® через 3 года после начала лечения.
Post hoc анализ показал 62% снижение относительного риска перелома бедра (1,4% снижение абсолютного риска, р < 0,01) у женщин > 75 лет, получавших лекарственное средство Пролиа®.
Влияние на все клинические переломы
Лечение препаратом Пролиа® значительно снижало частоту переломов всех типов/групп (смотрите таблицу 2 ниже).
Таблица 2 Влияние Пролиа® на риск клинических переломов после трех лет лечения
|
|
Количественное соотношение
женщин с переломами (%)+
|
Снижение
абсолютного риска (%)
(95% Cl)
|
Снижение
относительного риска (%)
(95% CI)
|
|
Плацебо n=3906
|
Пролиа® n=3902
|
|
Любой
клинический перелом1
|
10,2
|
7,2
|
2,9 (1,6, 4,2)
|
30 (19, 41)***
|
|
Клинический вертебральный перелом
|
2,6
|
0,8
|
1,8 (1,2, 2,4)
|
69 (53, 80)***
|
|
Невертебральный
перелом2
|
8,0
|
6,5
|
1,5 (0,3, 2,7)
|
20 (5, 33) **
|
|
Большой невертебральный перелом3
|
6,4
|
5,2
|
1,2 (0,1, 2,2)
|
20 (3, 34)*
|
|
Большой остеопоротический перелом4
|
8,0
|
5,3
|
2,7 (1,6, 3,9)
|
35 (22, 45) ***
|
*р ≤ 0,05; **р = 0,0106 (вторичная конечная точка, включенная в корректировку множества),
*** р ≤ 0,0001
*Частота возникновения побочной реакции на основе оценки Каплана-Мейера через 3 года.
1 Включая клинические вертебральные и невертебральные переломы.
2 За исключением переломов позвонков, черепа, нижней челюсти, пясти, фаланг пальцев руг и ног, лицевых переломов.
3 Включая переломы таза, дистального отдела бедра, проксимального отдела большеберцовой кости, ребер, проксимального отдела плечевой кости, костей предплечья и бедра.
4 Включая клинические вертебральные переломы, переломы бедра, костей предплечья, плечевой кости, в соответствии с определением ВОЗ.
У женщин с исходной минеральной плотностью кости шейки бедра ≤ -2,5. Пролиа® снижала риск невертебральных переломов (35% снижение относительного риска, 4,1% снижение абсолютного риска, р < 0,001, исследовательский анализ).
Снижение в частоте новых вертебральных переломов, переломов бедра и невертебральных переломов через 3 года приема препарата Пролиа® наблюдалось независимо от 10-летней вероятности возникновения переломов до начала лечения.
Влияние на минеральную плотность костей
Препарат Пролиа® значительно увеличивал минеральную плотность костей во всех анатомических областях, по сравнению с плацебо, через 1, 2 и 3 года лечения. Увеличение минеральной плотности кости наблюдалось на 9,2% в поясничном отделе позвоночника, на 6,0% в бедре, на 4,8% в шейке бедра, на 7,9% в вертеле бедренной кости, на 3,5% в дистальном отделе лучевой кости и на 4,1% в среднем во всех костях через 3 года после начала лечения (р < 0,0001 для всех значений).
В клинических исследованиях, оценивающих влияние отмены Пролиа®, минеральная плотность костей практически возвращалась к уровню до начала лечения и оставалась выше уровня плацебо в течение 18 месяцев после введения последней дозы. Полученные данные указывают на то, что для поддержания клинического эффекта требуется продолжительное лечение препаратом Пролиа®. Возобновление терапии препаратом Пролиа® приводило к увеличению минеральной плотности костей, схожим с тем, которое наблюдалось при первом введении препарата.
Открытое расширенное клиническое исследование лечения постменопаузального остеопороза
4550 пациентов (2343 получали Пролиа® и 2207 плацебо), которые пропустили не более одной дозы исследуемого препарата в базовом исследовании, описанном выше, и пришедшие на визит к врачу через 36 месяцев после начала исследования, согласились принять участие в семилетнем мультинациональном, мультицентровом, открытом, расширенном несравнительном исследовании долгосрочной безопасности и эффективности препарата Пролиа®. Все женщины в расширенном исследовании получали Пролиа® 60 мг каждые 6 месяцев, а также ежедневно принимали кальций (не менее 1 г) и витамин D (не менее 400 МЕ). В общей сложности 2626 пациентов (58% женщин, включенных в расширенное исследование, т.е. 34% женщин, включенных в базовое исследование) завершили расширенное исследование.
У пациентов, получавших Пролиа® на протяжение 10 лет исходная минеральная плотность костей увеличилась по сравнению с исходным уровнем в расширенном исследовании на 21,7% в поясничном отделе позвоночника, на 9,2% в бедре, на 9,0% в шейке бедра, на 13,0% в вертеле бедра и на 2,8% в дистальном отделе лучевой кости. Среднее значение Т-критерия минеральной плотности костей поясничного отдела позвоночника в конце исследования составляло -1,3 у пациентов, получавших лечение в течение 10 лет.
В качестве конечной точки безопасности оценивалась частота переломов, но эффективность в предотвращении переломов не может быть оценена из-за большого количества прекращения лечения и открытого дизайна исследования. Кумулятивная частота новых вертебральных и невертебральных переломов составила примерно 6,8% и 13,1% соответственно у пациентов, которые получали лечение деносумабом в течение 10 лет (n=1278). У пациентов, которые не завершили исследование по каким-либо причинам, наблюдалась более высокая частота переломов при лечении.
В ходе расширенного исследования было зафиксировано 13 подтвержденных случаев остеонекроза челюсти и 2 случая атипичных переломов шейки бедра.
Клиническая эффективность и безопасность у мужчин с остеопорозом
Эффективность и безопасность применения лекарственного средства Пролиа®, вводимого однократно каждые 6 месяцев, оценивалась в исследовании продолжительностью 1 год, включавшем 242 мужчин в возрасте от 31 до 84 лет. Из исследования были исключены лица с рСКФ (расчетная скорость клубочковой фильтрации) < 30 мл/мин/1,73 м
2. Все мужчины дополнительно получали кальций (не менее 1 000 мг) и витамин D (не менее 800 МЕ) ежедневно.
Первичной переменной эффективности являлось процентное изменение минеральной плотности кости в поясничном отделе позвоночника, эффективность в предотвращении переломов не оценивалась. Лекарственное средство Пролиа® значительно увеличило минеральную плотность кости во всех анатомических областях по сравнению с плацебо через 12 месяцев после начала лечения: на 4,8% в поясничном отделе, на 2,0% в бедре, на 2,2% в шейке бедра, на 2,3% в вертеле бедренной кости, на 0,9% в дистальном отделе лучевой кости (р < 0,05 для всех значений). Препарат Пролиа® увеличил минеральную плотность кости в поясничном отделе позвоночника по сравнению с исходным значением у 94,7% мужчин через год лечения. Значительное увеличение минеральной плотности кости в поясничном отделе, бедре, шейке бедра и вертеле бедренной кости наблюдалось через 6 месяцев после начала лечения (р < 0,0001).
Гистология костей у постменопаузальных женщин и мужчин с остеопорозом
Гистология костей оценивалась у 62 женщин с постменопаузальным остеопорозом или с низкой костной массой, которые ранее не проходили лечения по поводу остеопороза либо были переведены с терапии алендронатом с последующим применением препарата Пролиа® в течение 1-3 года. 59 женщин участвовали в исследовании с биопсией костей через 24 месяца (n=41) и/или 84 месяца (n=22) лечения в рамках расширенного клинического исследования у женщин с остеопорозом в постменопаузе. Гистология костей также оценивалась у 17 мужчин с остеопорозом через год лечения Пролиа®. Результаты биопсии костей показали нормальную архитектонику и качество кости без признаков нарушения минерализации, образования волокнистой кости или фиброза костного мозга. Результаты гистоморфометрии в расширенном исследовании у женщин в постменопаузе с остеопорозом показали, что антирезорбтивный эффект Пролиа®, который определялся по частоте активации и уровню формирования костной ткани, сохранялся в течение долгого времени.
Клиническая эффективность и безопасность у пациентов с потерей костной массы, вызванной депривацией андрогенов
Эффективность и безопасность Пролиа®, вводимого каждые 6 месяцев в течение трех лет, исследовались на мужчинах с гистологически подтвержденным неметастатическим раком предстательной железы, получающих андроген-депривационную терапию (1468 пациентов в возрасте 48-97 лет), которые были подвержены повышенному риску переломов (пациенты в возрасте > 70 лет, или пациенты в возрасте < 70 лет с минеральной плотностью костей в поясничном отделе, в бедре или шейке бедра Т-критерий < -1,0 или с наличием остеопоротических переломов в анамнезе). Все пациенты ежедневно получали кальций (не менее 1 000 мг) и витамин D (не менее 400 МЕ).
Препарат Пролиа® значительно увеличивал минеральную плотность костей во всех анатомических областях, по сравнению с плацебо, через 3 года лечения. Увеличение МПК наблюдалось на 7,9% в поясничном отделе позвоночника, на 5,7% в бедре, на 4,9% в шейке бедра, на 6,9% в вертеле бедренной кости, на 6,9% в дистальном отделе лучевой кости и на 4,7% во всем теле (р < 0,0001 для всех значений). В проспективно запланированном исследовательском анализе значительное увеличение минеральной плотности костей в поясничном отделе позвоночника, бедре, шейке бедра и вертеле бедренной кости наблюдалось через 1 месяц после введения начальной дозы.
Пролиа® продемонстрировала значительное снижение относительного риска новых вертебральных переломов: 85% (1,6% снижение абсолютного риска) через год, 69% (2,2% снижение абсолютного риска) через 2 года и 62% (2,4% снижение абсолютного риска) через 3 года (р < 0,01 для всех значений).
Клиническая эффективность и безопасность у пациентов с потерей костной массы, вызванной адъювантной терапией ингибиторами ароматазы
Эффективность и безопасность Пролиа®, вводимого каждые 6 месяцев в течение двух лет, оценивалась у женщин с неметастатическим раком молочной железы (252 пациентки в возрасте 35-84 лет) и исходными значениями минеральной плотности костей Т-критерий между -1,0 и -2,5 для поясничного отдела позвоночника, бедра или шейки бедра. Все женщины ежедневно дополнительно получали не менее 1 000 мг кальция и не менее 400 МЕ витамина D.
Первичной переменной эффективности являлось процентное изменение минеральной плотности костей в поясничном отделе позвоночника. Эффективность в отношении переломов не оценивалась. Препарат Пролиа® значительно увеличивал минеральную плотность костей во всех анатомических областях, по сравнению с плацебо, через 2 года лечения. Увеличение МПК наблюдалось на 7,6% в поясничном отделе позвоночника, на 4,7% в бедре, на 3,6% в шейке бедра, на 5,9 % в вертеле бедренной кости, на 6,1% в дистальном отделе лучевой кости и на 4,2% в среднем в костях (р < 0,0001 для всех значений).
Детская популяция
Европейское агентство по лекарственным средствам отказалось от обязательства представить результаты исследований Пролиа® во всех подгруппах детской популяции при лечении потери костной массы, связанной с аблативной терапией половыми гормонами, а также в подгруппе детского населения в возрасте до 2 лет при лечении остеопороза. Информацию о применении в детской популяции смотрите в разделе «Способ применения и дозы».
Фармакокинетика
Всасывание
После подкожного введения деносумаба в дозе 1,0 мг/кг, что приблизительно соответствует утвержденной дозе 60 мг, экспозиция, определяемая по площади под кривой концентрации (AUC) составила 78% в сравнении с внутривенным введением в той же дозе. При подкожном введении дозы 60 мг максимальная концентрация деносумаба (С
mах) в сыворотке – 6 мкг/мл (диапазон 1-17 мкг/мл) наблюдалась через 10 дней (диапазон 2-28 дней).
Биотрансформация
Деносумаб состоит из аминокислот и углеводов, как естественный иммуноглобулин, поэтому маловероятно, что препарат выводится через механизмы печеночного метаболизма. Ожидается, что метаболизм деносумаба будет происходить по пути клиренса иммуноглобулинов, с распадом на небольшие пептидные цепи и отдельные аминокислоты.
Выведение
После достижения С
mах содержание препарата в сыворотке крови снижалось с периодом полувыведения 26 дней (диапазон 6-52 дня) и далее в течение 3 месяцев (диапазон 1,5 4,5 месяцев). У 53% пациентов деносумаб не обнаруживался в сыворотке крови после 6 месяцев от последнего введения препарата.
Не наблюдалось изменений фармакокинетических параметров деносумаба, а также кумуляции за всё время введения многократных подкожных доз препарата по 60 мг каждые 6 месяцев. На фармакокинетику деносумаба не оказывало влияния формирование связывающих антител к деносумабу. Фармакокинетика была схожа у мужчин и женщин. Возраст (28-87 лет), раса, стадия заболевания (остеопения или остеопороз, рак предстательной или молочной железы) не оказывали значительного влияния на фармакокинетику деносумаба.
На основании показателей AUC и С
mах была выявлена тенденция к снижению экспозиции препарата у пациентов с более высокой массой тела. Однако данная тенденция не является клинически значимой, так как фармакодинамические эффекты, оцениваемые по маркерам ремоделирования кости и повышению минеральной плотности костей, оставались постоянными в различных весовых категориях больных.
Линейность/нелинейность
В ходе исследований по изучению дозозависимости была продемонстрирована нелинейная дозозависимая фармакокинетика деносумаба с уменьшением клиренса препарата при увеличении дозы или концентрации, но приблизительно пропорциональное дозозависимое увеличение экспозиции препарата наблюдается при применении доз 60 мг и выше.
Отдельные группы пациентов
Пациенты с почечной недостаточностью
В исследовании у 55 пациентов с различной степенью почечной дисфункции, включая пациентов, находящихся на диализе, степень почечной недостаточности не оказывала влияния на фармакокинетику деносумаба.
Печеночная недостаточность
Исследований влияния печеночной недостаточности на фармакокинетику деносумаба не проводилось. Как правило, моноклональные антитела не выводятся посредством механизмов печеночного метаболизма. Поэтому ожидается, что печеночная недостаточность не оказывает влияния на фармакокинетику деносумаба.
Применение у детей
Фармакокинетика у детей не изучалась.
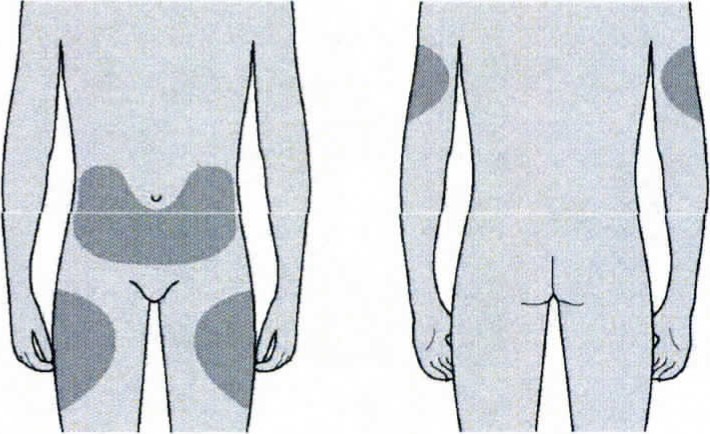
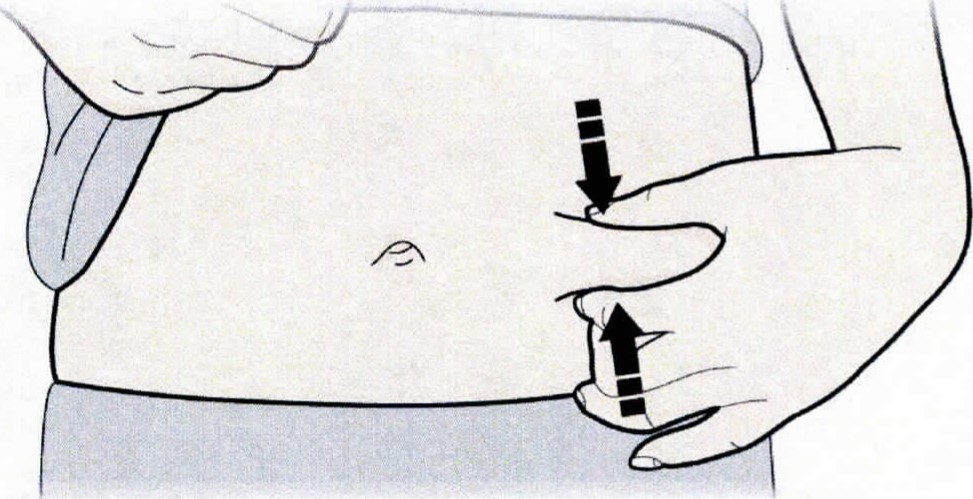
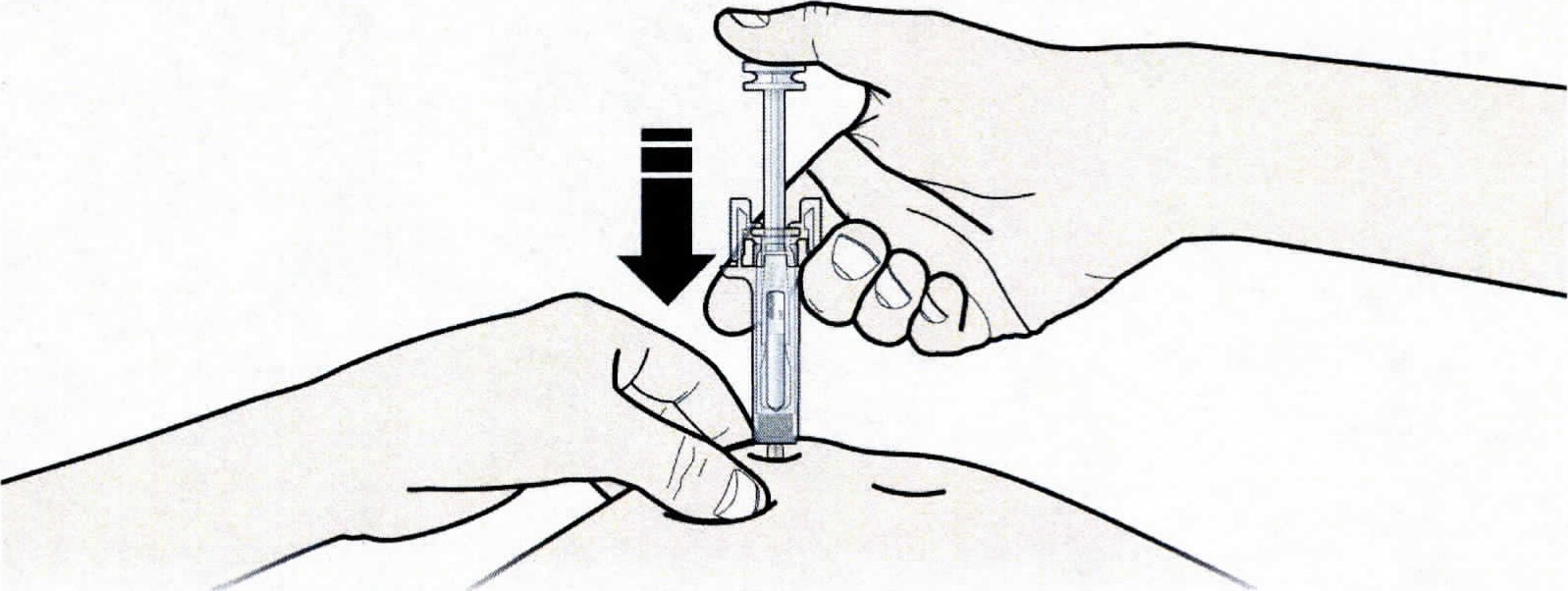
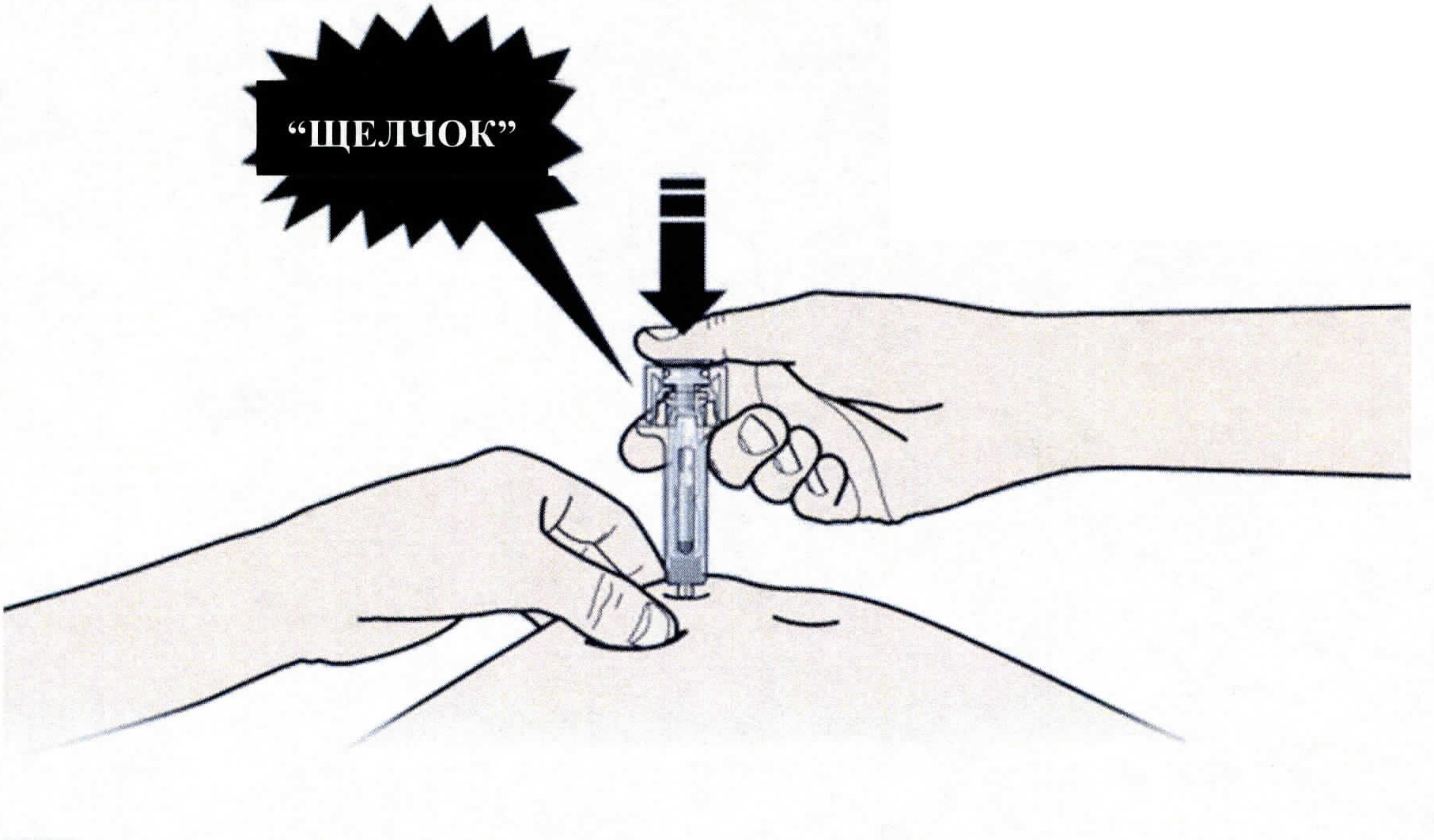
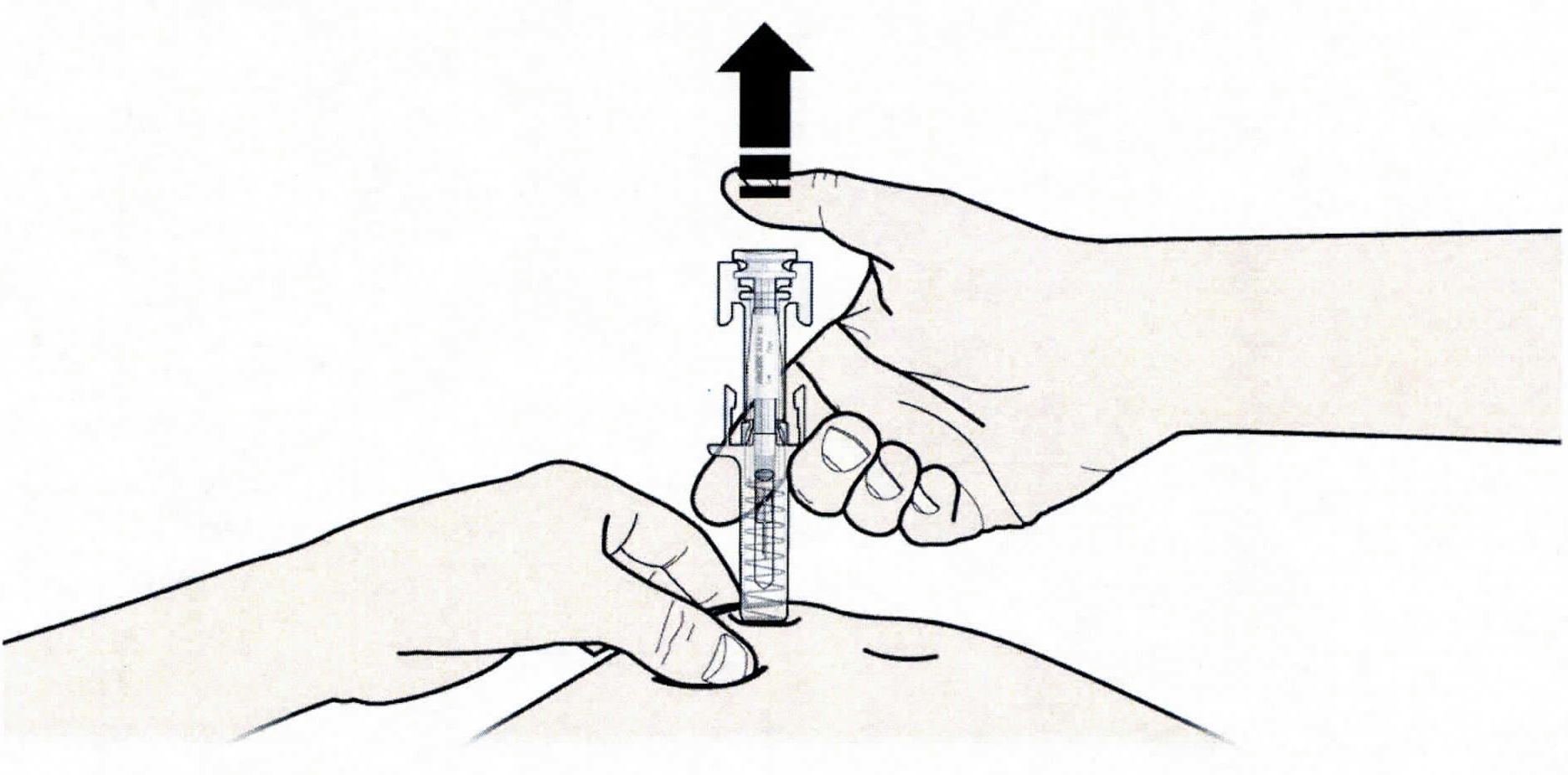
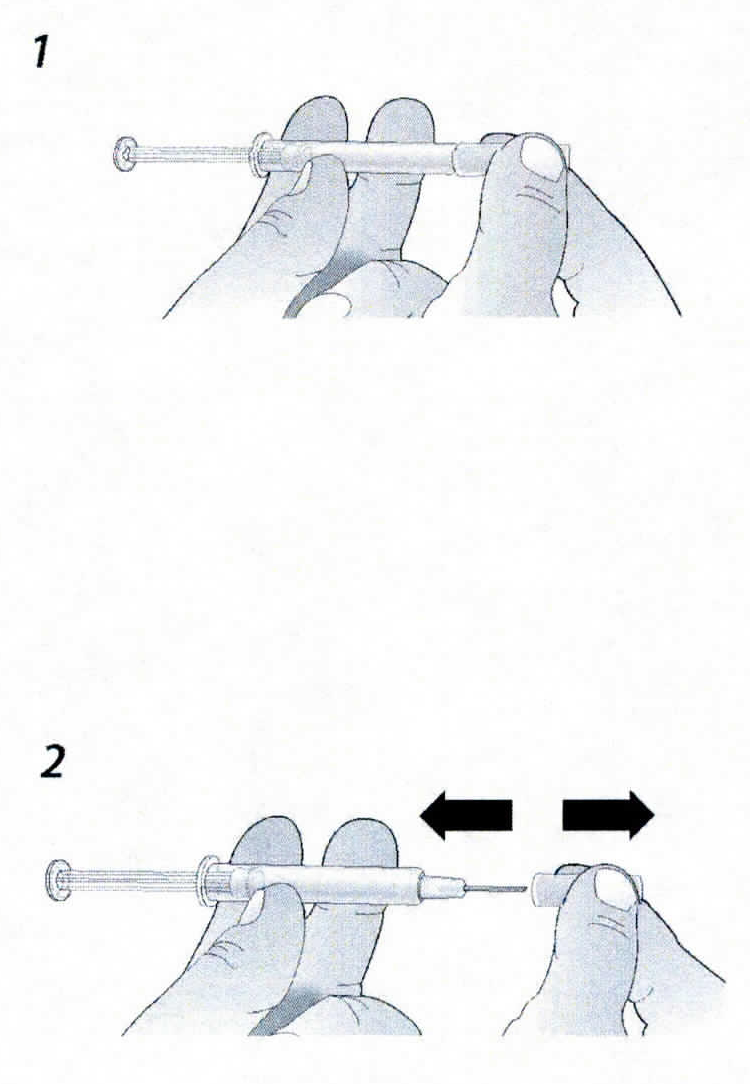 1. Продезинфицируйте место инъекции с помощью смоченного в спирте тампона.
1. Продезинфицируйте место инъекции с помощью смоченного в спирте тампона.