Кайендра: инструкция по применению
Форма выпуска: таблетки
Содержание
- Что из себя представляет препарат и для чего его применяют
- Показания к применению
- Противопоказания
- Особые указания и меры предосторожности
- Другие препараты и данный препарат
- Беременность, грудное вскармливание и фертильность
- Управление транспортными средствами и работа с механизмами
- Применение
- Передозировка
- Возможные нежелательные реакции
- Хранение и срок годности
- Состав
- Внешний вид препарата и содержимое упаковки
Что из себя представляет препарат и для чего его применяют
Препарат Кайендра® содержит действующее вещество сипонимод и принадлежит к группе препаратов под названием селективные иммунодепрессивные средства. Сипонимод является модулятором сфингозин-1-фосфатного рецептора (S1P).
Показания к применению
Препарат Кайендра® показан для лечения взрослых пациентов в возрасте 18 лет и старше с вторично-прогрессирующим рассеянным склерозом (ВПРС).
Способ действия препарата Кайендра®
Препарат Кайендра помогает защитить клетки центральной нервной системы (ЦНС) от атак собственной иммунной системы организма. Препарат осуществляет это за счет того, что:
- делает определенные лейкоциты (называемые лимфоцитами) менее способными свободно перемещаться в организме и
- предотвращает попадание этих клеток в головной и спинной мозг. Это уменьшает повреждение нервной системы, вызванное вторично-прогрессирующим рассеянным склерозом, и в результате препарат Кайендра® помогает замедлить развитие последствий заболевания (например, прогрессирование инвалидности, поражение головного мозга и обострения).
Если улучшение не наступило или Вы чувствуете ухудшение, необходимо обратиться к врачу.
Противопоказания
Не принимайте препарат Кайендра®:
- если у Вас аллергия на сипонимод, арахис, сою или любые другие компоненты препарата, перечисленные в разделе «Состав»;
- если у Вас синдром иммунодефицита (тяжелое нарушение работы иммунной системы);
- если у Вас когда-нибудь была прогрессирующая мультифокальная лейкоэнцефалопатия или криптококковый менингит;
- если у Вас есть активные злокачественные новообразования;
- если у Вас есть нарушение функции печени тяжелой степени (класс С по классификации Чайлд-Пью);
- если у Вас в течение предшествующих 6 месяцев были инфаркт миокарда, нестабильная стенокардия, инсульт/транзиторная ишемическая атака (ТИА) или определенные типы сердечной недостаточности (сердечная недостаточность в стадии декомпенсации (требующая стационарной терапии) или сердечная недостаточность класса III/IV по классификации Нью-Йоркской кардиологической ассоциации);
- если у Вас определенные типы нерегулярного или ненормального сердцебиения (атриовентрикулярная блокада II и III степеней типа Мобитц II, синоатриальная блокада, синдром слабости синусового узла в анамнезе), и Вы не используете электрокардиостимулятор;
- если анализы крови показывают, что Ваш организм не может достаточно хорошо расщеплять препарат (у Вас гомозиготный генотип изофермента CYPC9*3 (CYPC9*3*3)). Вы не должны его принимать (см. «Анализы до и во время лечения» ниже);
- если Вы беременны или обладаете сохраненным репродуктивным потенциалом (можете забеременеть), но не используете средства контрацепции (средства для предотвращения беременности);
Если Вы не уверены в том, что что-либо из перечисленного относится к Вам, проконсультируйтесь с лечащим врачом.
Особые указания и меры предосторожности
Перед применением препарата Кайендра® проконсультируйтесь с лечащим врачом:
- если у Вас инфекционное заболевание или Ваша иммунная система не работает должным образом (например, из-за болезни или Вы принимаете лекарственные препараты, подавляющие иммунную систему; см. также «Другие препараты и данный препарат»).
- если Вы никогда не болели ветряной оспой и не были привиты от нее. Вы можете подвергнуться большему риску осложнений, если во время лечения препаратом Кайендра® Вы заболеете ветряной оспой. Ваш лечащий врач может попросить Вас сделать прививку от ветряной оспы, прежде чем Вы начнете лечение.
- если Вы планируете вакцинироваться. Ваш лечаший врач проконсультирует Вас относительно вакцинации (см. «Другие препараты и данный препарат»).
- если у Вас когда-либо были или имеются проблемы со зрением (в частности, состояние, называемое макулярным отеком) или инфекция или воспаление глаза (увеит). Ваш лечащий врач может попросить Вас пройти осмотр глаз перед началом лечения и проходить его регулярно во время лечения. Препарат Кайендра® может вызвать отек макулы (области глаза, которая позволяет видеть формы, цвета и детали), который называется макулярным отеком. Вероятность развития макулярного отека выше, если он уже был у Вас ранее или если у Вас когда-либо был увеит (воспаление глаза).
- если у Вас сахарный диабет. Вероятность развития макулярного отека (см. выше) выше у пациентов с сахарным диабетом.
- если у Вас когда-либо было какое-либо из следующих состояний (даже если Вы получаете лечение от них): тяжелое заболевание сердца, нерегулярное или ненормальное сердцебиение (аритмия), инсульт или другое заболевание, связанное с кровеносными сосудами головного мозга, замедление сердечного ритма (брадикардия), обморок, нарушение сердечного ритма (о чем свидетельствуют отклонения от нормы результатов ЭКГ).
- если у Вас тяжелые нарушения дыхания во время сна (апноэ во сне).
- если у Вас высокое артериальное давление, которое невозможно контролировать с помощью лекарственных препаратов. Вам нужно будет регулярно проверять артериальное давление.
- если у Вас когда-либо были нарушения функции печени. Перед назначением препарата Кайедра Ваш лечащий врач может попросить Вас сдать анализы кровы, чтобы проверить как работает Ваша печень.
- если Вы можете забеременеть, поскольку сипонимод может нанести вред будущему ребенку при применении во время беременности. Прежде чем начать лечение, Ваш лечащий врач даст Вам пояснения относительно имеющегося риска и попросит пройти тест на беременность, чтобы убедиться, что Вы не беременны. Вы должны использовать эффективные методы контрацепции во время лечения и в течение 10 дней после прекращения лечения (см. «Беременность, грудное вскармливание и фертильность»).
Если что-либо из вышеперечисленного относится к Вам, сообщите об этом лечащему врачу, прежде чем принимать препарат Кайендра®.
Во время применения препарата Кайендра® следите за следующим
Если во время приема препарата Кайендра® у Вас возникнет что-либо из перечисленного ниже, немедленно сообщите об этом своему врачу, поскольку это может быть серьезным:
- Если у Вас инфекционное заболевание. Препарат Кайендра® снижает количество лейкоцитов в вашей крови. Лейкоциты борются с инфекциями, поэтому Вы можете легче заразиться пока принимаете препарат Кайендра® (и вплоть до 3-4 недель после прекращения приема). Данные инфекционные заболевания могут быть серьезными и, возможно, даже опасными для жизни.
- Если Вы считаете, что ваш рассеянный склероз прогрессирует (состояние ухудшается), или если Вы заметили какие-либо новые или необычные симптомы. Симптомы, схожие с ВПРС, могут быть вызваны очень редкой инфекцией головного мозга, которая называется прогрессирующей многоочаговой лейкоэнцефалопатией (ПМЛ). Данная инфекция может развиться у пациентов, принимающих такие лекарственные препараты, как Кайендра®, и другие лекарственные препараты, используемые для лечения рассеянного склероза.
- Если у Вас повышенная температура, вы чувствуете себя так, как будто заболели гриппом, или у Вас болит голова, скованность мышц шеи, чувствительность к свету, тошнота или спутанность сознания. Это могут быть симптомы менингита и/или энцефалита, вызванного вирусной или грибковой инфекцией (например, криптококковый менингит).
- Если у Вас появились такие симптомы как внезамная сильная головная боль, спутанность сознания, судороги и изменения зрения. Это могут быть симптомы состояния, называемого синдромом задней обратимой энцефалопатии (СЗОЭ).
- Если у Вас появились такие симптомы, как необъяснимая тошнота, рвота, боль в животе, усталость, пожелтение кожи или белков глаз или аномально темная моча. Это могут быть симптомы нарушений работы печени.
- Если Вы заметили какие-либо узелки на коже (например, блестящие, «жемчужные» узелки), пятна неправильной формы или открытые язвы, которые не заживают в течение нескольких недель.
Замедленный сердечный ритм (брадикардия) и нерегулярное сердцебиение
В течение первых дней лечения препарат Кайендра® может вызывать замедление частоты сердечных сокращений (брадикардию). Вы можете ничего не чувствовать или чувствовать головокружение или усталость. Это также может привести к тому, что Ваше сердцебиение станет нерегулярным в начале лечения. Если что-либо указывает на то, что Вы можете подвергаться более высокому риску возникновения данных эффектов, Ваш врач может принять решение о более тщательном наблюдении за Вами в начале лечения, сначала направить вас к кардиологу или отказаться от назначения Вам препарата Кайендра®.
Анализы до и во время лечения
То, как быстро препарат расщепляется (метаболизируется) в организме, меняется от пациента к пациенту, поэтому разным людям требуются разные дозы. Перед началом лечения врач попросит Вас сдать анализ крови или слюны, чтобы определить, какая доза Вам больше подходит. В редких случаях результат анализа может показать, что Вы не должны принимать препарат.
- Анализ крови
Желаемый эффект лечения препаратом Кайендра® заключается в уменьшении количества лейкоцитов в крови. Количество лейкоцитов обычно возвращается к нормальным значениям в течение 3-4 недель после прекращения лечения. Если Вам необходимо сдать анализы крови, сообщите врачу (который Вам их назначил), что Вы принимаете препарат Кайендра®. В противном случае врач не сможет корректно оценить результаты анализа, кроме того, для некоторых видов анализа крови может потребоваться отобрать больше крови, чем обычно.
До начала применения препарата Кайендра®, Вас попросят сдать анализ крови, чтобы проверить достаточно ли у Вас лейкоцитов в крови, кроме того, Ваш лечащий врач может также регулярно проводить данную проверку во время лечения. Если у Вас недостаточный уровень лейкоцитов, врач может потребовать прекратить прием или уменьшить дозу препарата Кайендра®.
Перед началом лечения Вам также проведут анализ крови, чтобы проверить работу Вашей печени.
Новообразования кожи
У пациентов с рассеянным склерозом, получивших леченине препаратом, были случаи возникновения новообразований кожи. Немедленно обратитесь к врачу, если Вы заметили какие-либо узелки на коже (например, блестящие «жемчужные» узелки), пятна с неровными краями или открытые язвы, которые не заживают в течение нескольких недель. Симптомы рака кожи могут включать необычный рост или изменения кожи (например, необычные родинки), характеризующиеся изменением цвета, формы или размера с течением времени. Перед началом приема препарата необходимо провести обследование кожи, чтобы проверить наличие подозрительных поражений кожи. Во время лечения препаратом Кайендра® Ваш врач также будет проводить регулярные осмотры кожи. Если у вас появятся проблемы с кожей, Ваш лечащий врач может направить Вас к дерматологу, который после консультации может решить, что Вам необходимо регулярное наблюдение.
Воздействие солнца и защита от солнца
Препарат Кайендра® ослабляет вашу иммунную систему. Это может увеличить риск развития рака кожи. Вы должны ограничить воздействие солнца и УФ-лучей на свой организм следующим образом:
- носить соответствующую защитную одежду,
- регулярно применять солнцезащитные крема с высокой степенью защиты от ультрафиолета.
Обострение рассеянного склероза после прекращения лечения препаратом Кайендра®
Не прекращайте прием препарата Кайендра® и не изменяйте дозу без предварительной консультации с лечащим врачом. Немедленно сообщите своему врачу, если Вы считаете, что Ваше состояние ухудшилось после прекращения лечения препаратом (см. «Прекращение приема препарата Кайендра®» в разделе «Применение»).
Пожилые пациенты (65 лет и старше)
Опыт применения препарата у пациентов пожилого возраста отсутствует. Проконсультируйтесь со своим врачом, если у Вас есть какие-либо опасения. Следует соблюдать осторожность при применении препарата у пожилых пациентов.
Дети и подростки
Не давайте препарат детям и подросткам младше 18 лет, так как исследования по применению препарата в данной возрастной группе не проводились.
Препарат Кайендра® содержит соевый лецитин и лактозы моногидрат
Препарат содержит соевый лецитин. Если у Вас аллергия на арахис или сою, не применяйте этот лекарственный препарат.
Препарат содержит лактозы моногидрат. Если у Вас непереносимость некоторых сахаров, обратитесь к лечащему врачу перед приемом данного лекарственного препарата.
Другие препараты и данный препарат
Сообщите лечащему врачу или работнику аптеки о том, что Вы принимаете, недавно принимали или можете начать принимать какие-либо другие препараты.
Сообщите лечащему врачу, если Вы принимаете лекарственные препараты или проходите терапию, указанные ниже:
- препараты для лечения нарушений сердечного ритма (антиаритмические средства), такие как, например, амиодарон, прокаинамид, хинидин или соталол. Лечащий врач может решить не назначать Вам препарат Кайендра, поскольку он может усилить влияние на нерегулярное сердцебиение.
- препараты, замедляющие частоту сердечных сокращений, такие как, например, верапамил, дилтиазем (относятся к группе лекарственных препаратов, которые называются блокаторами кальциевых каналов), ивабрадин, дигоксин. Ваш врач может направить Вас к кардиологу, после чего Вам, возможно, потребуется заменить принимаемый препарат, поскольку Кайендра® также может замедлять частоту сердечных сокращений в первые дни лечения. Если Вы принимаете бета- адреноблокаторы, такие как атенолол или пропранолол, лечащий врач может попросить Вас временно прекратить терапию бета-адреноблокаторами до тех пор, пока вы не достигнете полной (поддерживающей) суточной дозы препарата Кайендра®.
- препараты, влияющие на иммунную систему, такие как химиопрепараты, иммунодепрессанты или другие препараты для лечения рассеянного склероза. Ваш врач может попросить Вас прекратить их прием, чтобы избежать усиления воздействия на иммунную систему.
- вакцины. Если Вам необходима вакцинация, то перед этим Вы должны проконсультироваться со своим врачом. Во время и в течение 4 недель после прекращения применения препарата Кайендра® Вам не следует применять определенные типы вакцин (называемые живыми аттенуированными вакцинами), поскольку они могут спровоцировать инфекцию, которую они должны были предотвратить (см. раздел 2).
- флуконазол и некоторые другие лекарственные препараты могут повышать уровень препарата Кайендра® в крови, и их не рекомендуется принимать в сочетании с препаратом Кайендра®. Ваш врач проконсультирует вас по данному вопросу.
- карбамазепин и некоторые другие лекарственные препараты могут снижать уровень препарата Кайендра® в крови и, как следствие, препятствовать его действию. Ваш врач проконсультирует вас по данному вопросу.
- модафинил и некоторые другие лекарственные препараты могут снижать уровень препарата Кайендра® в крови некоторых пациентов и, как следствие, препятствовать его действию. Ваш врач проконсультирует вас по данному вопросу, если это будет Вам применимо.
- фототерапия УФ-излучением или ПУВА-фотохимиотерапия. УФ-терапия во время лечения препаратом Кайендра® может увеличить риск развития рака кожи.
Беременность, грудное вскармливание и фертильность
Если Вы беременны или кормите грудью, думаете, что забеременели, или планируете беременность, перед началом применения препарата Кайендра® проконсультируйтесь с лечащим врачом или работником аптеки.
Не принимайте препарат Кайендра® во время беременности, если Вы пытаетесь забеременеть или если Вы можете забеременеть и не используете надежные методы контрацепции. Применение препарата Кайендра во время беременности повышает риск нарушения развития (врожденных пороков) у ребенка. Перед началом лечения препаратом Кайендра® лечащий врач попросит Вас сдать тест на беременность, чтобы убедиться, что Вы не беременны. Вы должны использовать надежные методы контрацепции во время лечения препаратом Кайендра® и как минимум в течение 10 дней после приема последней дозы препарата.
Если Вы забеременели во время лечения препаратом Кайендра®, немедленно обратитесь к лечащему врачу. Он отменит терапию (см. «Если Вы прекратили прием препарата Кайендра®»). Вам будет назначено необходимое пренатальное (дородовое) обследование.
Вы не должны кормить грудью во время приема препарата Кайендра®. Препарат Кайендра® может проникать в грудное молоко, и существует риск серьезных побочных эффектов для ребенка.
Влияние сипонимода на фертильность человека не оценивалось.
Управление транспортными средствами и работа с механизмами
Ваш врач проконсультирует Вас о том, позволяет ли Ваша болезнь безопасно управлять транспортными средствами и работать с механизмами. Препарат Кайендра® оказывает несущественное влияние на способность управлять транспортными средствами и работать с механизмами или не оказывает его вовсе. Однако в начале лечения может возникать головокружение. Не управляйте транспортными средствами и не работайте с механизмами в первый день приема препарата Кайендра®.
Применение
Терапию препаратом Кайендра® должен начинать и контролировать врач, имеющий опыт лечения рассеянного склероза.
Всегда принимайте препарат в полном соответствии с рекомендациями лечащего врача. При появлении сомнений посоветуйтесь с лечащим врачом.
Рекомендуемая доза
Начало лечения
Лечение начинают со стартовой упаковки препарата Кайендра®, рассчитанной на 5 дней, в течение которых Ваша доза будет постепенно увеличиваться, см. ниже таблицу «Стартовая упаковка».
Целью постепенного увеличения дозы (фазы титрации) является снижение риска побочных эффектов на сердце в начале лечения. Ваш врач может внимательно наблюдать за Вашим состоянием в начале лечения, если у Вас есть риск замедления или нерегулярности сердечного ритма.
Стартовая упаковка
| День терапии | Доза | Количество таблеток препарата Кайендра® в дозе 0,25 мг, которое необходимо принять |
| День 1 | 0,25 мг | 1 таблетках0,25 мг |
| День 2 | 0,25 мг | 1 таблетках0,25 мг |
| День 3 | 0,50 мг | 2 таблетких0,25 мг |
| День 4 | 0,75 мг | 3 таблетких0,25 мг |
| День 5 | 1,25 мг | 5 таблетокх0,25 мг |
На 6 день Вы начнете принимать Вашу обычную поддерживающую дозу.
В течение первых 6 дней начала терапии рекомендуемую дозу препарата следует принимать один раз в сутки утром независимо от приема пищи.
Поддерживающая доза
Рекомендуемая поддерживающая доза составляет 2 мг (1 таблетка препарата Кайендра® по 2 мг) независимо от приема пищи.
Ваш врач может назначить Вам прием только 1 мг один раз в сутки (четыре таблетки препарата Кайендра® по 0,25 мг), если анализ крови, проведенный до начала лечения, показал, что Ваш организм медленно расщепляет препарат Кайендра® (см. «Анализы до и во время лечения»). Если это относится к Вам, то обратите внимание, что прием пяти таблеток по 0,25 мг на 5-й день фазы титрации, как указано выше, является безопасным для Вас.
Пациенты пожилого возраста
Следует соблюдать осторожность при применении препарата у пожилых пациентов.
Пациенты с нарушением функции почек
Не требуется коррекции дозы препарата у пациентов с нарушением функции почек.
Пациенты с нарушением функции печени
Препарат противопоказан у пациентов с нарушением функции печени тяжелой степени (класс С по классификации Чайлд-Пью). Несмотря на то, что не требуется коррекции дозы препарата у пациентов с нарушением функции печени легкой и средней степеней тяжести, следует соблюдать осторожность при начале терапии препаратом у пациентов данной группы.
Путь и (или) способ введения
Препарат принимают внутрь, запивая водой.
Продолжительность терапии
Принимайте препарат так долго, как рекомендует лечащий врач.
Если Вы забыли принять препарат Кайендра®
Если Вы забыли принять дозу в один из первых 6 дней лечения, то сообщите об этом Вашему лечащему врачу. Лечение нужно будет начать заново со дня 1 (с новой стартовой упаковки).
Если Вы пропустили прием поддерживающей дозы (начиная с 7-го дня лечения), назначенную дозу следует принять в следующее по графику время приема; следующую дозу не следует удваивать, чтобы компенсировать пропущенную дозу. В случае если Вы пропустили прием поддерживающей дозы препарата Кайендра® в течение 4 или более последовательных дней, сообщите об этом Вашему лечащему врачу, лечение нужно будет начать заново со дня 1 (с новой стартовой упаковки).
Если Вы прекратили прием препарата Кайендра®
Не прекращайте прием препарата Кайендра® и не меняйте Вашу дозу, не проконсультировавшись с лечащим врачом.
Препарат Кайендра® будет оставаться в организме до 10 дней после прекращения его приема. Количество лимфоцитов может оставаться низким в течение 3-4 недель после прекращения приема препарата Кайендра®. Применение иммуносупрессантов (лекарственных препаратов, подавляющих иммунную систему) в этот период может приводить к развитию дополнительного угнетающего воздействия на иммунную систему, в связи с чем следует соблюдать осторожность в течение 3-4 недель после приема последней дозы сипонимода. Нежелательные реакции, описанные в данном листке- вкладыше, могут проявиться и в этот период (см. «Возможные нежелательные реакции»)
Если Вам потребуется возобновить прием препарата Кайендра® более чем через 4 дня после прекращения его приема, Ваш врач назначит Вам новую стартовую упаковку (для титрования дозы), и Вам потребуется начать лечение заново со дня 1.
Если Вы считаете, что после прекращения лечения препаратом Кайендра® Ваш рассеянный склероз прогрессирует (состояние ухудшается), немедленно сообщите об этом своему врачу.
При наличии вопросов по применению препарата обратитесь к лечащему врачу.
Передозировка
Если Вы приняли слишком много таблеток препарата Кайендра® или если Вы приняли Вашу первую таблетку из упаковки с поддерживающей дозой вместо таблетки из стартовой упаковки, немедленно сообщите об этом своему врачу. В подобных случаях врач может принять решение наблюдать за Вашим состоянием.
Возможные нежелательные реакции
Подобно всем лекарственным препаратам, препарат Кайендра® может вызывать нежелательные реакции, однако они возникают не у всех.
Некоторые нежелательные реакции, которые могут быть серьезными
Часто (могут возникать не более чем у 1 человека из 10)
- Сыпь с небольшими пузырьками, неполненными жидкостью, появляющаяся на покрасневшей коже (симптомы вирусной инфекции, называемой опоясывающим герпесом, которая может быть тяжелой)
- Тип рака кожи, называемый базальноклеточной карциномой (БКК), который часто проявляется в виде «жемчужного» узелка, хотя может принимать и другие формы.
- Лихорадка, боль в горле и/или язвы во рту, вызванные инфекцией (лимфопения)
- Судороги, припадки
- Нарушения зрения, такие как тень или слепое пятно в центре поля зрения, затуманенное зрение, нарушения распознавания цветов или деталей (симптомы макулярного отека, представляющего собой отек в макулярной области сетчатки в задней части глаза)
- Нерегулярное сердцебиение (атриовентрикулярная блокада)
- Замедленное сердцебиение (брадикардия)
Нечасто (могут возникать не более чем у 1 из 100 человек)
- Тип рака кожи, называемый плоскоклеточным раком, который может проявляться в виде твердого красного узелка, язвы с коркой или новой язвы на существующем рубце.
Редко (могут возникать не более чем у 1 из 1000 человек)
- Инфекция головного мозга, называемая прогрессирующей мультифокальной лейкоэнцефалопатией (НМЛ). Симптомы НМЛ могут быть похожи на симптомы рассеянного склероза, такие как слабость или изменения зрения, потеря памяти, трудности с мышлением или трудности при ходьбе.
Частота неизвестна (невозможно оценить частоту по доступным данным)
- Криптококковые инфекции (разновидность грибковой инфекции) или вирусные инфекции (вызванные вирусом герпеса или ветряной оспы), включая менингит и или энцефалит с такими симптомами, как головная боль со скованностью шейных мышц, чувствительностью к свету, плохим самочувствием (тошнотой) или спутанностью сознания.
Если у вас возникнут какие-либо из вышеуказанных нежелательных реакций, немедленно сообщите об этом своему врачу.
Другие возможные нежелательные реакции, которые могут наблюдаться при приеме препарата Кайендра®
Другие нежелательные реакции включают перечисленные ниже. Если какая-либо из указанных ниже нежелательных реакций становится серьезной, сообщите об этом своему врачу.
Очень часто (могут возникать более чем у 1 человека из 10)
• высокое артериальное давление (артериальная гипертензия), иногда с такими симптомами как головная боль и головокружение;
• увеличение показателей функции печени
Часто (могут возникать не более чем у 1 человека из 10)
• головокружение
• непроизвольное сотрясение тела (тремор)
• диарея
• плохое самочувствие (тошнота)
• боль в руках или ногах
• отек рук, лодыжек, ног или ступней (периферический отек)
• слабость(астения)
• снижение показателей функции легких.
Сообщение о нежелательных реакциях
Если у Вас возникают какие-либо нежелательные реакции, проконсультируйтесь с врачом или работником аптеки. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в листке-вкладыше. Вы также можете сообщить о нежелательных реакциях напрямую через систему сообщения государства-члена Евразийского экономического союза. Сообщая о нежелательных реакциях, Вы помогаете получить больше сведений о безопасности препарата.
Российская Федерация:
Адрес: 109012, г. Москва, Славянская площадь, д. 4, стр. 1
Телефон: +7 (800) 550-99-03
Электронная почта: pharm@roszdravnadzor.gov.ru
Сайт в информационно-телекоммуникационной сети «Интернет»: https://www.roszdravnadzor.gov.ru
Республика Казахстан:
Адрес: 010000, г. Астана, ул. А.Иманова, 13, 4 этаж
Телефон: +7 7172 235 135
Электронная почта: farm@dari.kz, pdlc@dari.kz, vigilance@dari.kz
Сайт: www.ndda.kz
Республика Беларусь:
Адрес: 220037, г. Минск, пер. Товарищеский, 2а
Телефон: +375 (17) 242-00-29
Факс: +375 (17) 242-00-29
Электронная почта: rcpl@rceth.by
Сайт: https://www.rceth.by
Хранение и срок годности
Храните препарат в недоступном для ребенка месте так, чтобы ребенок не мог увидеть его.
Не применяйте препарат после истечения срока годности (срока хранения), указанного на упаковке. Датой истечения срока годности является последний день месяца.
Хранить при температуре от 2 до 8 °С.
После получения препарата хранить при температуре не выше 25 °С не более 3 месяцев.
Не выбрасывайте препарат в канализацию. Уточните у работника аптеки, как следует утилизировать (уничтожать) препарат, который больше не потребуется. Эти меры позволят защитить окружающую среду.
Состав
Препарат Кайендра® содержит
Действующим веществом является сипонимод.
Кайендра®, 0,25 мг, таблетки, покрытые пленочной оболочкой
Каждая таблетка содержит 0,250 мг сипонимода (в виде сипонимода фумарата (сипонимод и фумаровая кислота, сокристалл).
Прочими ингредиентами (вспомогательными веществами) являются лактозы моногидрат, целлюлоза микрокристаллическая, кросповидон (тип А), глицерил дибегенат, кремния диоксид коллоидный, поливиниловый спирт частично гидролизованный, титана диоксид (Е171), тальк, лецитин соевый (Е322), камедь ксантановая, краситель железа оксид красный (Е172), краситель железа оксид черный (Е172).
Кайендра®, 2 мг, таблетки, покрытые пленочной оболочкой
Каждая таблетка содержит 2,000 мг сипонимода (в виде сипонимода фумарата (сипонимод и фумаровая кислота, сокристалл).
Прочими ингредиентами (вспомогательными веществами) являются лактозы моногидрат, целлюлоза микрокристаллическая, кросповидон (тип А), глицерил дибегенат, кремния диоксид коллоидный, поливиниловый спирт частично гидролизованный, титана диоксид (Е171), тальк, лецитин соевый (Е322), камедь ксантановая, краситель железа оксид красный (Е172), краситель железа оксид желтый (Е172).
Внешний вид препарата и содержимое упаковки
Таблетки, покрытые пленочной оболочкой
Кайендра®, 0,25 мг, таблетки, покрытые пленочной оболочкой
Круглые, двояковыпуклые таблетки, покрытые пленочной оболочкой светло-красного цвета, со скошенными краями, без риски, с гравировкой «Т» на одной стороне и «(!)» - на другой.
По 12 таблеток, покрытых пленочной оболочкой, в блистер из ПА / Ал / ПВХ и алюминиевой фольги. По 1 блистеру в картонном пенале вместе с листком-вкладышем (инструкцией по медицинскому применению) в картонную пачку («стартовая упаковка») или по 10 блистеров вместе с листком-вкладышем (инструкцией по медицинскому применению) в картонную пачку.
Кайендра®. 2 мг, таблетки, покрытые пленочной оболочкой
Круглые, двояковыпуклые таблетки, покрытые пленочной оболочкой светло-желтого цвета, со скошенными краями, без риски, с гравировкой «II» на одной стороне и «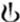 » - на другой.
» - на другой.
По 14 таблеток, покрытых пленочной оболочкой, в блистер из ПА / Ал / ПВХ и алюминиевой фольги. По 2 блистера вместе с листком-вкладышем (инструкцией по медицинскому применению) в картонную пачку.
Допускается наличие контроля первого вскрытия на картонной пачке.
Держатель регистрационного удостоверения
4056 Базель, Лихтштрассе 35, Швейцария.
Производитель
Шаффхаузерштрассе, 4332 Штейн, Швейцария / Schaffhauserstrasse, 4332 Stein, Switzerland, или
Новартис Фарма ГмбХ / Novartis Pharma GmbH
90429, Роонштрассе 25 и Обере Турнштрассе 8-10, Нюрнберг, Германия / 90429, Roonstrasse
25 und Obere Tumstrasse 8-10, Nurnberg, Germany
ил и (для дозировки 2 мг)
Общество с ограниченной ответственностью «Новартис Нева» (ООО «Новартис Нева»)
г. Санкт-Петербург, Дорога в Каменку, д. 40, к. 3, лит. А, Российская Федерация.
За любой информацией о препарате, а также в случаях возникновения претензий следует обращаться к местному представителю держателя регистрационного удостоверения:
Российская Федерация
Адрес: 125315, г. Москва, Ленинградский проспект, д. 70
Телефон: +7 495 967 12 70
Факс: +7 495 967 12 68
Электронная почта: drug.safety_russia@novartis.com
Республика Казахстан
Адрес: 050022, г. Алматы, ул. Курмангазы, 95
Телефон: +7 727 258 24 47
Электронная почта: drugsafety.cis@novartis.com
Республика Беларусь
Республике Беларусь
Адрес: 220069, г. Минск, пр-т Дзержинского, 5, пом. 3, офис 3-1
Телефон: +375 (17)360 03 65
Электронная почта: drugsafety.cis@novartis.com
Прочие источники информации
Подробные сведения о данном препарате содержатся на веб-сайте Союза http://еес.eaeunion.org/.