Лечение должно проводиться врачом, имеющим опыт лечения гемофилии.
Дозы и длительность заместительной терапии зависят от степени тяжести дефицита фактора свертывания крови VIII, локализации и тяжести кровотечения, а также клинического состояния пациента. Количество единиц вводимого фактора VIII измеряется в международных единицах (ME), что соответствует действующему стандарту Всемирной Организации Здравоохранения (ВОЗ) для препаратов, содержащих фактор свертывания крови VIII. Активность фактора VIII в плазме выражается в процентах (относительно нормальной плазмы человека) или в ME (относительно международного стандарта содержания фактора VIII в плазме).
Одна ME активности фактора VIII эквивалентна количеству фактора VIII в одноммиллилитре нормальной плазмы крови человека.
Расчёт необходимой дозы фактора VIII основывается на эмперически выявленной закономерности, согласно которой 1 МЕ фактора VIII на килограмм массы тела повышает активность плазматического фактора VIII приблизительно на 2 % ( или 2 МЕ/дл) от исходной активности.
Необходимая доза рассчитывается по следующей формуле.
Необходимое количество единиц = масса тела [кг] × требуемое повышение фактора VIII [% или МЕ/дл] × 0,5.
Доза и частота введений всегда должны рассчитываться с учетом клинической эффективности в каждом индивидуальном случае.
В случаях кровотечений, приведенных в таблице ниже, активность фактора VIII за соответствующий период не должна быть ниже указанного в таблице уровня активности плазмы (в % от нормального уровня или в МЕ/дл).
Таблица расчета доз препарата при кровотечениях и в хирургической практике
|
Тяжесть кровотечения / тип хирургической процедуры
|
Необходимый уровень фактора VIII (% или МЕ/дл)
|
Частота введения доз (часы) / продолжительность терапии (дни)
|
|
Кровотечение:
|
|
|
|
Ранний гемартроз, мышечное или ротовое кровотечение
|
20-40
|
Повторные инфузии препарата каждые 12-24 часа.
Как минимум 1 день, до тех пор, пока не остановится кровотечение (по болевым ощущениям) или не наступит заживление.
|
|
Более массивное кровотечение, мышечное кровотечение или гематома
|
30-60
|
Повторные инфузии препарата каждые 12-24 часа в течение 3-4 дней или более, до тех пор, пока болевой синдром или выраженная недееспособность не исчезнут.
|
|
Жизнеугрожающее кровотечение
|
60-100
|
Повторные инфузии каждые 8-24 часа до устранения угрозы для жизни.
|
|
Хирургия:
|
|
|
|
Малая, включая удаление зуба
|
30-60
|
Каждые 24 часа, как минимум 1 день, пока не наступит заживление.
|
|
Большая
|
80-100 (до и после операции)
|
Повторные инфузии каждые 8-24 часа до адекватного заживления раны, затем терапия на протяжении не менее 7 дней для поддержания активности фактора VIII на уровне 30-60% (МЕ/дл).
|
Во время курса лечения для расчета вводимой дозы и частоты инфузий рекомендуется определять уровень фактора VIII. Существует значительная индивидуальная вариабельность ответа на лечение фактором VIII, in vivo демонстрируя разные показатели восстановления и периоды полувыведения. Расчитанная на основе массы тела доза может требовать корректировки для пациентов с недостаточным или избыточным весом. При обширном хирургическом вмешательстве проведение мониторинга заместительной терапии при помощи коагуляционного анализа (активность плазматического фактора VIII) является обязательным.
Профилактика
При долгосрочной профилактике кровотечений у пациентов с тяжелой формой гемофилии А обычно применяется фактор VIII в дозе 20-40 МЕ/кг массы тела с интервалом введения 2-3 дня. В некоторых случаях, особенно у молодых пациентов, могут потребоваться более короткие интервалы и/или более высокие дозы.
Особые группы пациентов
Расчет доз препарата производится исходя из массы тела, поэтому при определении доз у детей применяются те же формулы расчета, что и у взрослых. При определении частоты введения препарата должна учитываться клиническая эффективность в каждом отдельном случае. Существует некоторый опыт лечения детей младше 6 лет.
Поскольку клинический опыт применения Бериате® у ранее нелеченных пациентов очень ограничен, безопасность и эффективность применения Бериате® у таких пациентов не установлена.
С помощью клинических наблюдений и анализов необходимо проводить контроль вырабатывания ингибиторов фактора свертывания крови VIII у пациентов, проходящих лечение препаратами фактора VIII. Если при применении препарата не удается достигнуть ожидаемого уровня активности фактора VIII или остановить кровотечение при введении рассчитанной дозы, необходимо провести анализ на наличие ингибиторов фактора VIII. У пациентов с высоким содержанием ингибиторов терапия фактором VIII может оказаться неэффективной, и в таких случаях должно рассматриваться альтернативное лечение. Ведение таких пациентов должно осуществляться врачами, имеющими опыт лечения пациентов больных гемофилией и пациентов с ингибиторами к фактору VIII.
Инструкция по приготовлению раствора
Общие инструкции
1. Раствор восстановленного лиофилизата варьируется от прозрачного до слегка опалесцирующего. После фильтрации и перед введением рекомендуется визуально проконтролировать восстановленный препарат на наличие частиц и изменения окраски. Не применяйте мутный раствор или раствор, содержащий осадок и/или включения.
2. Откупоривание, восстановление раствора и забор в шприц должны производится в асептических условиях.
3. Остатки препарата и упаковку после использования следует утилизировать в соответствии с местными требованиями.
Восстановление раствора
Нагреть растворитель до комнатной температуры. Убедиться, что крышки с флаконов с растворителем и препаратом удалены, пробки обработаны антисептическим раствором и просушены до открытия устройства для добавления растворителя со встроенным фильтром*.

|
1. Откройте блистерную упаковку устройства для добавления растворителя со встроенным фильтром путем удаления верхней части упаковки. Не вынимайте устройство из блистерной упаковки!
|
|
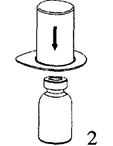
2. Поместите флакон с растворителем на ровную чистую поверхность и крепко держите флакон. Возьмите устройство для добавления растворителя со встроенным фильтром вместе с блистерной упаковкой и острым стержнем синей части устройства проткните пробку флакона с растворителем, надавливая вертикально вниз.
|
|
3. Аккуратно снимите блистерную упаковку с устройства для добавления растворителя, удерживая ее за края и потянув вертикально вверх. Убедитесь в том, что вы удалили только блистерную упаковку, а не само устройство.
|

|
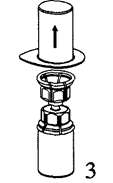
4. Поместите флакон с препаратом на твердую ровную поверхность. Переверните над ним флакон с растворителем вместе с прикрепленным к нему устройством для добавления растворителя и острым стержнем прозрачной части устройства проткните пробку флакона с препаратом, надавливая вертикально вниз. Растворитель автоматически переместится во флакон с препаратом.
|
|
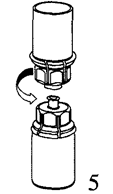
5. Крепко удерживая одной рукой устройство для добавления растворителя со стороны флакона с препаратом, а другой рукой – со стороны флакона из-под растворителя, аккуратно развинтите устройство на две части. Флакон из-под растворителя с синей частью устройства следует выбросить.
|
|
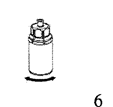
6. Аккуратно покрутите флакон с препаратом с прикрепленной прозрачной частью устройства до полного растворения лиофилизата. Не встряхивайте флакон.
|

|
7. Наберите воздух в пустой стерильный шприц и, удерживая флакон с препаратом в вертикальном положении, присоедините шприц к наконечнику Люэра на устройстве для добавления растворителя со встроенным фильтром. Введите воздух во флакон с раствором препарата.
|
Забор и утилизация препарата
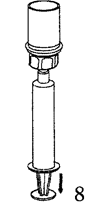
|
8. Нажимая на поршень шприца, переверните флакон вместе со шприцем, и затем, плавно оттягивая поршень шприца, наберите в него восстановленный раствор препарата.
|

|
9. После того, как восстановленный раствор препарата набран в шприц, обхватите цилиндр шприца (удерживая шприц вниз поршнем) и отсоедините прозрачную часть устройства для добавления растворителя от шприца.
|
*Устройство для добавления растворителя со встроенным фильтром предназначено для одноразового использования; не использовать устройство в случае повреждения упаковки и после истечения срока годности, который указан на бумажной части блистерной упаковки следующим образом: «ЕХР. год-месяц»
Для инъекций препарата Бериате® рекомендуется использовать одноразовые пластиковые шприцы, поскольку раствор может остаться на стеклянных стенках цельностеклянных шприцев. Раствор препарата следует нагреть до комнатной температуры или температуры тела перед введением. Препарат следует вводить медленно внутривенно со скоростью, не причиняющей дискомфорт пациенту, предварительно убедившись в том, что кровь не попадает в шприц с препаратом. Скорость введения препарата не должна превышать 2 мл в минуту.
Следует внимательно наблюдать за пациентом на предмет развития у него аллергической реакции немедленного типа. Если у пациента наблюдается реакция, которая может быть вызвана введением Бериате, необходимо уменьшить скорость введения препарата или прекратить введение в зависимости от клинического состояния пациента.
Восстановленный раствор остается химически и физически стабильным в течение 8 часов при температуре 25 °C. Однако, с точки зрения биологической стабильности, восстановленный раствор должен вводиться немедленно после разведения. Хранение восстановленного раствора не должно превышать 8 часов при комнатной температуре.








