Противопоказания
Индивидуальная гиперчувствительность к октреотиду или любому из вспомогательных веществ, в т.ч. компонентам растворителя.
Способ применения и дозы
Сандостатин ЛАР следует вводить исключительно путем глубокой внутримышечной инъекции в ягодичную мышцу. Место повторных мышечных инъекций следует чередовать путем введения в правую и левую ягодичные мышцы.
Для обеспечения применения правильной дозировки температура комплекта Сандостатина ЛАР (порошок и раствор) должна быть выровнена с комнатной температурой перед приготовлением суспензии (см. раздел «Инструкция по приготовлению суспензии и выполнению внутримышечной инъекции Сандостатин ЛАР»).
Акромегалия
Терапию рекомендуется начинать с введения 20 мг Сандостатина ЛАР с 4-недельными интервалами в течение 3 месяцев. Если пациент получал лечение Сандостатином, введение Сандостатина ЛАР можно начинать на следующий день после последнего подкожного введения дозы Сандостатина. Последующую корректировку дозирования следует основывать на уровне гормона роста (ГР) в сыворотке крови, концентрациях инсулиноподобного фактора роста 1/соматомедина С (IGF 1), а также клинических признаках заболевания.
Для пациентов, у которых в пределах этого 3-месячного периода клинические симптомы и биохимические параметры (ГР; IGF 1) контролируются не в полной мере (концентрации гормона роста ГР остаются выше 2,5 мкг/л), дозу можно увеличить до 30 мг каждые 4 недели.
Пациентам, у которых после 3 месяцев применения 20 мг концентрации ГР стали существенно ниже 1 мкг/л, нормализовались концентрации IGF 1 в сыворотке крови и исчезли наиболее обратимые симптомы акромегалии, можно вводить 10 мг Сандостатина ЛАР каждые 4 недели. Однако в такой группе пациентов при введении этой низкой дозы Сандостатина ЛАР рекомендовано усиление адекватного контроля концентраций ГР и IGF 1, а также клинических признаков.
У пациентов, получающих стабильную дозу Сандостатина ЛАР, оценку уровня ГР и IGF 1 следует проводить каждые 6 месяцев.
Эндокринные опухоли желудочно-кишечного тракта и поджелудочной железы
Лечение пациентов с симптомами функциональных эндокринных опухолей ЖКТ и поджелудочной железы
Рекомендуется начать лечение таких пациентов с введения Сандостатина подкожно в дозе 0,1 мг 3 раза в день в течение короткого периода (около 2-х недель) с целью оценки эффективности и системной переносимости октреотида перед началом применения Сандостатина ЛАР.
Терапию Сандостатином ЛАР рекомендуется начинать с введения 20 мг Сандостатина ЛАР с 4-недельными интервалами. Пациентам, получающим лечение Сандостатином, рекомендуется продолжить подкожное введение Сандостатина в прежней эффективной дозе в течение 2 недель после первой инъекции Сандостатина ЛАР.
Для пациентов, у которых симптомы и биологические маркеры после 3 месяцев лечения должным образом контролируются, дозу можно уменьшить до 10 мг Сандостатина ЛАР каждые 4 недели.
Для пациентов, у которых симптомы лишь частично контролируются после 3 месяцев лечения, дозу можно увеличить до 30 мг Сандостатина каждые 4 недели.
В те дни, когда в ходе лечения Сандостатином ЛАР усиливаются симптомы, связанные с опухолями желудочно-кишечного тракта и поджелудочной железы, рекомендовано дополнительное подкожное введение Сандостатина в дозе, применяемой до терапии Сандостатином ЛАР. Эта ситуация может возникнуть главным образом в первые 2 месяца лечения до достижения терапевтических концентраций октреотида.
Лечение пациентов с распространенными нейроэндокринными опухолями средней (тонкой и толстой) кишки или с неизвестной локализацией первичной опухоли
Рекомендуемая доза Сандостатина ЛАР составляет 30 мг каждые 4 недели. Лечение Сандостатином ЛАР для контроля опухоли должно продолжаться при отсутствии прогрессирования опухоли.
Особые группы пациентов
Применение у пациентов с нарушенной функцией почек
Нет необходимости в корректировке дозы Сандостатина ЛАР (см.раздел «Фармакокинетика»).
Применение у пациентов с нарушенной функцией печени
У пациентов с циррозом печени может снижаться способность к выведению октреотида из организма, однако это не происходит у пациентов с жировым гипатозом (см. раздел «Фармакокинетика»). Ввиду широкого терапевтического диапазона октреотида отсутствует необходимость в корректировке дозы Сандостатина ЛАР у пациентов с циррозом печени.
Применение у пожилых пациентов (≥65 лет)
Отсутствует необходимость в корректировке дозы Сандостатина ЛАР у данной группы пациентов.
Применение у детей.
Опыт применения препарата Сандостатин ЛАР у детей органичен.
Информацию о приготовлении суспензии для внутримышечного введения и руководство по применению см. в конце инструкции.
Побочное действие
В клинических исследованиях при применении октреотида наиболее частыми наблюдаемыми побочными реакциями на препарат были диарея, боль в животе, тошнота, метеоризм, головная боль, холелитиаз, гипергликемия и запор. Другие часто сообщаемые нежелательные реакции были представлены головокружением, локализованной болью, билиарным сладжем, дисфункцией щитовидной железы (например, снижение уровня тиреотропного гормона [ТТГ], уменьшение концентрации общего и свободного Т4), послабляющим стулом, нарушением толерантности к глюкозе, рвотой, астенией и гипогликемией.
В редких случаях побочные эффекты со стороны ЖКТ могут напоминать острую кишечную непроходимость с прогрессирующим вздутием живота, сильной болью в эпигастрии, болезненностью живота. Несмотря на то, что может увеличиваться выделяемое с калом количество жира, к настоящему времени нет свидетельств того, что длительная терапия октреотидом может привести к недостаточному питанию по причине нарушения всасывания. В очень редких случаях сообщалось о развитии острого панкреатита по истечении первых нескольких часов или суток терапии Сандостатином п/к. После отмены препарата явление разрешалось. Кроме того, у пациентов, получавших длительную терапию Сандостатином п/к, сообщались случаи панкреатина, вызванного холелитиазом.
У пациентов наблюдались изменения на ЭКГ, такие как удлинение интервала QT, поворот электрической оси, ранняя реполяризация, уменьшение вольтажа, переход R/S, раннее прогрессирование зубца R и неспецифические изменения зубцов ST-T. Связь между этими явлениями с применением октреотида ацетата достоверно не установлена, поскольку многие из этих пациентов страдали другими заболеваниями сердца (см. раздел Меры предосторожности).
Сводная информация о нежелательных лекарственных реакциях по данным клинических исследований и постмаркетингового наблюдения
Наблюдались следующие побочные реакции, приведенные согласно классификации MedDRA в порядке снижения частоты. Категории частоты: очень часто (≥ 1/10); часто (≥ 1/100, < 1/10); нечасто (≥ 1/1,000, < 1/100); редко (≥ 1/10,000, < 1/1,000); очень редко (< 1/10,000), частота не известна (спонтанные сообщения и обзор литературных данных при постмаркетинговом применении). В каждой группе побочные реакции расположены в порядке уменьшения их серьезности.
Нарушения со стороны иммунной системы. Частота не известна: анафилактическая реакция, аллергия/реакции гиперчувствительности.
Нарушения со стороны желудочно-кишечной системы. Очень часто - диарея, боль в животе, тошнота, метеоризм, запор; часто - диспепсия, рвота, вздутие живота, стеаторея, послабляющий стул, обесцвечивание каловых масс.
Нарушения со стороны нервной системы. Очень часто - головная боль, часто - головокружение.
Нарушения со стороны эндокринной системы. Часто гипотиреоз, дисфункция щитовидной железы (например, снижение уровня ТСГ, снижение уровня общего Т4, снижение уровня свободного Т4).
Нарушения со стороны гепатобилиарной системы. Очень часто - холелитиаз; часто - холецистит, гипербилирубинемия; частота не известна - острый панкреатит, острый гепатит без холестаза, холестатический гепатит, холестаз, желтуха, холестатическая желтуха.
Нарушения обмена веществ и питания. Очень часто - гипергликемия; часто - гипогликемия, нарушение толерантности к глюкозе, снижение аппетита; нечасто - обезвоживание.
Общие нарушения и нарушения в месте введения. Очень часто - реакция в месте инъекции; часто - астения.
Лабораторные показатели. Часто - повышение уровней трансаминаз печени; частота не известна - увеличение щелочной фосфатазы в крови, увеличение гамма-глутамилтрансферазы.
Нарушения со стороны кожи и подкожной клетчатки. Часто - зуд, сыпь, алопеция; частота не известна - крапивница.
Нарушения со стороны дыхательной системы. Часто - одышка.
Нарушения со стороны сердечно-сосудистой системы. Часто - брадикардия; нечасто - тахикардия; частота не известна - аритмия.
Нарушения со стороны крови и лимфатической системы. Частота не известна - тромбоцитопения.
Описание отдельных нежелательных реакций
Реакции, связанные с желчным пузырем
Было показано, что аналоги соматостатина ингибируют сократимость желчного пузыря и снижают секрецию желчи, что может привести к нарушениям со стороны желчного пузыря или образованию сладжа.
Возникновение камней в желчном пузыре было отмечено у 15-30% пациентов, получающих Сандостатин подкожно в течение длительного периода времени. Распространенность этой патологии в общей популяции (в возрасте от 40 до 60 лет) составляет около 5-20%. Долгосрочная экспозиция Сандостатина ЛАР пациентов с акромегалией или гастроэнтеропанкреатическими опухолями предполагает, что лечение Сандостатином ЛАР не увеличивает частоту образования желчных камней по сравнению с подкожным введением. В случае образования желчных камней обычно симптомы отсутствуют; при клинических проявлениях желчнокаменную болезнь следует лечить с использованием холелитических препаратов или хирургическими методами.
Тромбоцитопения
Сообщалось о случаях тромбоцитопении в пострегистрационном периоде, особенно во время применения препарата Сандостатин (в/в) у пациентов с циррозом печени и препарата Сандостатин ЛАР. Она обратима при прекращении лечения.
Передозировка
Сообщали об ограниченном числе случайных передозировок Сандостатином ЛАР. Дозы находились в диапазоне от 100 мг до 163 мг/месяц Сандостатина ЛАР. Единственным побочным явлением были приливы.
Сообщали о пациентах, больных раком, которые получали дозы Сандостатина ЛАР вплоть до 60 мг/месяц и до 90 мг/2 недели. Эти дозы в целом хорошо переносились; однако сообщали о следующих побочных явлениях: частое мочеиспускание, утомляемость, депрессия, тревога, потеря концентрации внимания.
Лечение: симптоматическое.
Беременность, грудное вскармливание, фертильность
Беременность
Достоверных и хорошо контролируемых исследований применения препарата у беременных женщин не проводилось. В постмаркетинговых исследованиях сообщали об ограниченном числе беременных пациенток с акромегалией, которым вводили препарат, однако в половине случаев исход беременности неизвестен. Большинству женщин вводили октреотид в первый триместр беременности в дозах в диапазоне от 100 до 300 мкг/сутки Сандостатина подкожно или от 20 до 30 мг/месяц Сандостатина ЛАР. Приблизительно в 2/3 случаев с известным исходом женщины предпочли продолжить лечение октреотидом во время беременности. В большинстве случаев с известным исходом родились здоровые дети, но есть сообщения о нескольких спонтанных абортах в первом триместре беременности, и нескольких случаях искусственного прерывания беременности.
В случаях с известным исходом беременности отсутствовали случаи врожденных пороков или аномалий развития, обусловленные применением октреотида.
Исследования на животных не выявило токсических воздействий на течение беременности, развитие эмбриона/плода, течение родов или постнатальное развитие, за исключением временного замедления физиологического роста.
Сандостатин ЛАР следует назначать беременным только по строгим показаниям.
Грудное вскармливание
Неизвестно, проникает ли октреотид с грудным молоком у человека. В исследованиях на животных было показано, что октреотид проникает в грудное молоко. При необходимости применения Сандостатина ЛАР грудное вскармливание на время лечения следует прекратить.
Фертильность
Неизвестно, влияет ли октреотид на фертильность у человека. Октреотид не снижает фертильность у самцов и самок крыс в дозах до 1 мг/кг/сутки.
Меры предосторожности
Общие
Поскольку иногда опухоли гипофиза, секретирующие гормон роста, могут увеличиваться, вызывая серьезные осложнения (например, сужение поля зрения), существенным является тщательный мониторинг состояния пациентов. В случае появления признаков увеличения опухоли следует рассмотреть необходимость применения альтернативных видов лечения.
Терапевтическая польза снижения уровня гормона роста (ГР) и нормализация концентрации инсулиноподобного фактора роста 1 (IGF-1) у женщин с акромегалией потенциально могут восстановить фертильность. Во время лечения октреотидом женщинам детородного возраста следует рекомендовать применение адекватных методов контрацепции.
У пациентов, получающих длительную терапию октреотидом, следует контролировать функцию щитовидной железы.
Явления, связанные с сердечно-сосудистой системой
Сообщали о частых случаях брадикардии. Может понадобиться корректировка дозы таких препаратов, как бета-блокаторы, блокаторы кальциевых каналов, препараты, контролирующие водный обмен или электролитный баланс.
Явления, связанные с желчным пузырем
Холелитиаз (желчнокаменная болезнь) - это явление, очень часто отмечающееся во время лечения препаратом Сандостатин, она может быть ассоциирована с холециститом и расширением желчных протоков (см. раздел «Побочное действие»).
Рекомендуется проведение ультразвукового исследования желчного пузыря перед началом терапии Сандостатином ЛАР и каждые 6 месяцев в ходе лечения.
Метаболизм глюкозы
Вследствие угнетающего действия на секрецию гормона роста, высвобождение глюкагона и инсулина, Сандостатин ЛАР может нарушать регуляцию уровня глюкозы. Возможно нарушение толерантности к глюкозе после приема пищи. В некоторых случаях в результате постоянного введения может возникнуть персистирующая гипергликемия, как это наблюдали у пациентов при подкожном введении Сандостатина. Имелись также сообщения о гипогликемии.
У пациентов с сопутствующим сахарным диабетом 1 типа Сандостатин ЛАР может влиять на регуляцию глюкозы, снижая потребность в инсулине. У пациентов без сахарного диабета и с сахарным диабетом 2 типа с частично нарушенной секрецией инсулина подкожное введение Сандостатина может увеличивать гликемию после приема пищи. В связи с этим рекомендуется контролировать толерантность к глюкозе и противодиабетическое лечение. Поскольку октреотид по сравнению с инсулином оказывает относительно большее ингибирующее влияние на секрецию гормона роста и глюкагона, а также в связи с меньшей длительностью ингибирующего воздействия на секрецию инсулина, у пациентов с инсулиномой октреотид может увеличивать степень тяжести и продолжительность гипогликемии. Состояние таких пациентов следует тщательно контролировать.
Питание
Октреотид может нарушать у некоторых пациентов всасывание жиров.
В некоторых случаях при лечении октреотидом наблюдали снижение уровня витамина В12 и отклонения от показателей теста Шиллинга. У пациентов с авитаминозом витамина В12 в анамнезе следует контролировать уровень этого витамина в ходе терапии Сандостатином ЛАР.
Влияние на скорость реакции при управлении автотранспортом или другими механизмами
Отсутствуют данные о влиянии Сандостатина ЛАР на способность управлять автотранспортом и другими механизмами.
Взаимодействие с другими лекарственными препаратами и другие виды взаимодействий
При одновременном применении с Сандостатином ЛАР может потребоваться коррекция доз лекарственных средств, влияющих на водный обмен и баланс электролитов, таких как бета-блокаторы, блокаторы кальциевых каналов и препараты, контролирующие водный обмен или электролитный баланс (см. раздел Меры предосторожности).
При одновременном применении с Сандостатином ЛАР может потребоваться коррекция доз инсулина и противодиабетических препаратов (см. раздел Меры предосторожности).
Установлено, что октреотид снижает всасывание циклоспорина в кишечнике и замедляет всасывание циметидина.
Одновременное введение октреотида и бромокриптина увеличивает биодоступность бромокриптина.
Ограниченные опубликованные данные свидетельствуют о том, что аналоги соматостатина могут снижать метаболический клиренс веществ, метаболизируемых ферментами цитохрома Р-450, что может быть обусловлено угнетением гормона роста. Поскольку нельзя исключить аналогичный эффект при применении октреотида, следует соблюдать осторожность при применении других препаратов, метаболизирующиеся главным образом CYP3A4 и обладающих узким терапевтическим диапазоном (например, хинидин, терфенадин).
Фармакологические свойства
Фармакодинамика
Октреотид - синтетический октапептид, являющийся производным естественного гормона соматостатина со сходными фармакологическими эффектами и значительно большей продолжительностью действия. Пептид угнетает патологически повышенную секрецию гормона роста (ГР), а также пептидов и серотонина, продуцируемых в гастроэнтеропанкреатической (ГЭП) эндокринной системе.
В опытах на животных октреотид является более мощным ингибитором секреции ГР, глюкагона и высвобождения инсулина, чем соматостатин, с большей селективностью относительно угнетения ГР и глюкагона.
У здоровых добровольцев октреотид, подобно соматостатину, подавляет:
- высвобождение ГР, стимулированное аргинином, физической нагрузкой и инсулиновой гипогликемией,
- высвобождение инсулина, глюкагона, гастрина, других пептидов гастроэнтеропанкреатической (ГЭП) эндокринной системы, вызываемое приемом пищи, а также высвобождение инсулина и глюкагона, стимулированное аргинином,
- высвобождение тиреотропного гормона (ТТГ), стимулированное тиреолиберином (TRH).
В отличие от соматостатина, октреотид в большей степени ингибирует секрецию гормона роста, его введение не сопровождается рикошетной гиперсекрецией гормонов (т.е. гормона роста у пациентов с акромегалией).
У пациентов с акромегалией Сандостатин ЛАР, применяемый для повторных введений с интервалами в 4 недели, обеспечивает постоянные терапевтические уровни октреотида в сыворотке крови, последовательно снижая уровень гормона роста и нормализуя концентрацию инсулиноподобного фактора роста 1 в сыворотке крови большинства пациентов. У большинства пациентов Сандостатин ЛАР заметно уменьшает клинические проявления болезни, такие как головная боль, потоотделение, парестезия, утомляемость, остеоартралгия и запястный сухожильный синдром. У значительной части (50%) нелеченных ранее пациентов с акромегалией, имеющих аденому гипофиза, секретирующую гормон роста, лечение Сандостатином ЛАР привело к уменьшению объема опухоли на > 20%.
У пациентов с функциональными эндокринными опухолями желудочно-кишечного тракта и поджелудочной железы лечение Сандостатином ЛАР обеспечивает постоянный контроль симптомов, связанных с основным заболеванием. Действие октреотида на различные типы опухолей желудочно-кишечного тракта и поджелудочной железы описано ниже.
Карциноидные опухоли:
Введение октреотида может привести к облегчению симптомов, в частности, приливов и диареи. Во многих случаях это сопровождается снижением концентрации серотонина в плазме крови и уменьшением выведения 5-гидроксииндолуксусной кислоты с мочой.
ВИПомы:
Биохимической характеристикой данных опухолей является избыточный синтез вазоактивного интестинального пептида (ВИП). В большинстве случаев введение октреотида приводит к ослаблению тяжелой секреторной диареи, типичной при данной патологии. Это сопровождается уменьшением сопутствующих нарушений в электролитном балансе, например, гипокалиемии, что позволяет отменить энтеральное и парентеральное введение жидкости и электролитов. У некоторых больных по данным компьютерной томографии происходит замедление или прекращение прогрессирования опухоли и даже уменьшение ее размеров, особенно метастазов в печень. Клиническое улучшение обычно сопровождается снижением (вплоть до нормальных значений) концентрации ВИП в плазме крови.
Глюкагономы:
Введение октреотида приводит в большинстве случаев к существенному уменьшению некротизирующей мигрирующей сыпи, характерной для данного состояния. Окреотид не оказывает сколько-нибудь какого-либо существенного влияния на выраженность сахарного диабета, часто наблюдающегося при глюкагономах и обычно не приводит к снижению потребности в инсулине или пероральных сахароснижающих препаратах. У больных, страдающих диареей, октреотид вызывает уменьшение ее тяжести, что сопровождается увеличением массы тела.
При применении октреотида часто отмечается быстрое снижение концентрации глюкагона в плазме крови, однако при длительном лечении этот эффект не сохраняется. В то же время симптоматическое улучшение остается стабильным в течение длительного времени.
Гастриномы/синдром Золлингера-Эллисона:
Несмотря на то, что терапия ингибиторами протонного насоса или селективными блокаторами гистаминовых Н2-рецепторов позволяет предотвратить повторное образование пептических язв вследствие хронической гастринстимулируемой гиперсекреции соляной кислоты, это лечение может оказаться недостаточно эффективным. Диарея может оказаться существенным симптомом, который не уменьшается у всех пациентов при применении данной терапии. Октреотид, применяемый в качестве монотерапии или в комбинации с ингибиторами протонного насоса или блокаторами Н2-гистаминовых рецепторов, может снизить продукцию соляной кислоты в желудке и привести к клиническому улучшению, включая диарею. Возможно также уменьшение выраженности и других симптомов, вероятно, обусловленных синтезом пептидов опухолью, в том числе приливов. У некоторых пациентов отмечается снижение концентрации гастрина в плазме крови.
Инсулиномы:
Введение октреотида снижает уровень иммунореактивного инсулина в крови. У пациентов с операбельной опухолью октреотид может обеспечить восстановление и поддержание нормогликемии в предоперационный период. У пациентов с неоперабельными доброкачественными и злокачественными опухолями контроль гликемии может улучшаться и без одновременного продолжительного снижения уровня инсулина в крови.
Соматолибериномы:
Эти редкие опухоли характеризуются продукцией только рилизинг фактора гормона роста - соматолиберина (GRF) или в комплексе с другими активными пептидами. Октреотид уменьшает выраженность симптомов акромегалии. Это, вероятно, обусловлено ингибированием секреции соматолиберина (GRF) и гормона роста, а также уменьшением гипертрофии гипофиза.
Фармакокинетика
Фармакокинетический профиль октреотида после инъекции Сандостатина ЛАР отображает профиль высвобождения октреотида из полимерной матрицы и ее биодеградацию. Сразу после высвобождения в системный кровоток октреотид распределяется согласно своим фармакокинетическим свойствам, описанным для подкожного введения.
После однократной внутримышечной инъекции Сандостатина ЛАР концентрация октреотида в сыворотке крови достигает начального пика в течение одного часа после введения, с последующим постепенным снижением до уровня октреотида ниже предела обнаружения в течение 24 часов. В первый день происходит высвобождение менее 0,5% от общего количества препарата. У большинства пациентов в течение следующих 7 дней после введения препарата концентрация октреотида остается на субтерапевтическом уровне. Концентрация октреотида достигает плато приблизительно на 14 день, и остается на таком уровне в течение последующих 3-4 недель. Примерно через 42 дня концентрация октреотида начинает медленно уменьшатся из-за терминальной деградации полимерной матрицы лекарственной формы.
Распределение
Объем распределения октреотида составляет 0,27 л/кг и общий клиренс составляет 160 мл/мин. Связывание с белками плазмы крови достигает 65%. Связывание октреотида с клетками крови крайне незначительно.
Выведение
Период полувыведения после подкожного введения составляет 100 мин. Большая часть пептида выводится с фекалиями, примерно 32 % выводится в неизменном виде с мочой.
Фармакокинетика у особых групп пациентов
Нарушение функции почек
Нарушение функции почек не оказывает влияния на общую экспозицию (AUC) октреотида при его подкожном введении.
Нарушение функции печени
При циррозе печени, но не при жировом гепатозе печени, выведение октреотида из организма снижается на 30%.
Несовместимость.
Сандостатин ЛАР, порошок для приготовления раствора для внутримышечного введения предназначен для индивидуального применения, без какого-либо разведения другими препаратами. В связи с этим отсутствуют данные по совместимости с другими препаратами.
Срок годности
3 года. Не допускается применять препарат после окончания срока годности, указанного на упаковке.
Условия хранения
Хранить при температуре от 2 °C до 8 °C в оригинальной упаковке для защиты от света. Хранить в недоступном для детей месте.
Суспензию следует готовить исключительно непосредственно перед внутримышечной инъекцией.
Упаковка
Порошок в стеклянном флаконе, закрытом резиновой пробкой, обжатой алюминиевым колпачком с крышкой flip-off синего (дозировка 10 мг), оранжевого (дозировка 20 мг) или красного (дозировка 30 мг) цвета в комплекте с растворителем, иглой для инъекций и адаптером для флакона.
Растворитель 2,0 мл раствора в предварительно наполненном стеклянном шприце.
Адаптер для флакона и игла для инъекций индивидуально упакованы в блистеры.
1 флакон с порошком, 1 шприц с растворителем, адаптер для флакона и игла для инъекций помещены в пластиковый трей. Трей вместе с инструкцией по применению упакован в картонную пачку.
Категория отпуска
По рецепту.
Производители.
Сандоз ГмбХ, Австрия;
Новартис Фарма Штейн АГ, 4332 Штейн, Шаффшаузерштрассе, Швейцария
Инструкции по приготовлению суспензии и выполнению внутримышечной инъекции Сандостатина ЛАР
ТОЛЬКО ДЛЯ ГЛУБОКОЙ ВНУТРИМЫШЕЧНОЙ ИНЪЕКЦИИ В ЯГОДИЧНУЮ ОБЛАСТЬ
Упаковка препарата содержит:
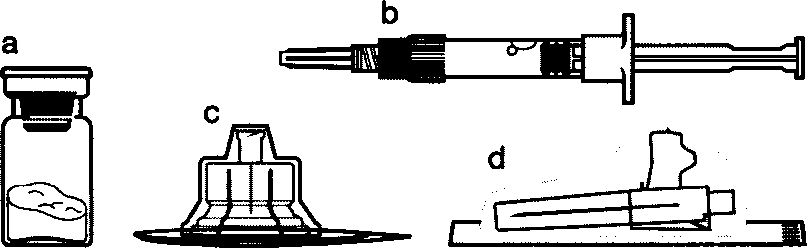
a) флакон с порошком Сандостатин ЛАР
b) шприц, заполненный растворителем
c) адаптер для флакона
d) безопасная инъекционная игла
Тщательно следуйте приведенным ниже указаниям, чтобы обеспечить надлежащее приготовление препарата Сандостатин ЛАР для глубокой внутримышечной инъекции.
В приготовлении препарата Сандостатин ЛАР есть три критически важных требования.
Нарушение этих правил может привести к невозможности соответствующим образом ввести препарат.
•
Набор для инъекции необходимо довести до комнатной температуры. Извлеките из холодильника набор для инъекции и выдержите его перед приготовлением суспензии при комнатной температуре в течение не менее 30 минут, но не более 24 часов.
• После добавления растворителя оставьте флакон стоять в течение 5 минут, чтобы растворитель гарантированно
полностью пропитал порошок.
• После насыщения
умеренно встряхивайте флакон в горизонтальном направлении в течение не менее 30 секунд для
получения однородной суспензии. Суспензию Сандостатин ЛАР следует приготовить только
непосредственно перед введением.
Инъекцию Сандостатин ЛАР должен проводить только обученный медработник.
Этап 1.
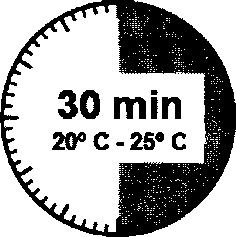
• Комплект Сандостатин ЛАР следует достать из холодильника.
ВНИМАНИЕ: Очень важно
начинать приготовление суспензии только после того, как температура комплекта сравняется с комнатной. Для этого необходимо выдержать флакон и растворитель перед приготовлением при комнатной температуре в течение не менее 30 минут, но не более 24 часов.
Примечание: при необходимости комплект можно снова поместить в холодильник.
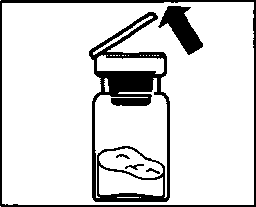 Этап 2.
Этап 2.
• Снимите пластиковую цветную крышку с флакона и протрите спиртовым тампоном резиновую пробку флакона.
• Снимите пленку, закрывающую адаптер для флакона в упаковке, но НЕ ВЫНИМАЙТЕ адаптер для флакона из упаковки.
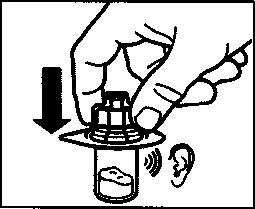
• Удерживая упаковку адаптера для флакона, поместите адаптер для флакона на верхнюю часть флакона и нажмите на него до упора так, чтобы он встал на место, при этом должен раздаться щелчок.
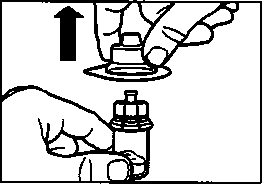
• Снимите вертикальным движением упаковку с адаптера для флакона.
 Этап 3.
Этап 3.
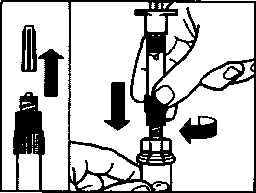
• Снимите колпачок с заполненного растворителем шприца и привинтите шприц к адаптеру для флакона.
• Медленно нажимая вниз на поршень, введите весь растворитель во флакон.
 Этап 4.
ВНИМАНИЕ: Очень важно оставить флакон стоять
Этап 4.
ВНИМАНИЕ: Очень важно оставить флакон стоять в течение 5 минут, чтобы растворитель гарантированно полностью пропитал порошок.
Примечание: Возможно движение поршня шприца вверх, поскольку во флаконе может быть небольшое избыточное давление.
• За это время подготовьте пациента к инъекции.
 Этап 5.
Этап 5.
• После периода насыщения убедитесь, что поршень в шприце доведен вниз до упора.
ВНИМАНИЕ: Удерживая поршень нажатым, умеренно встряхивайте флакон в горизонтальном направлении в течение
не менее 30 секунд для получения однородной молочной суспензии. Убедитесь, что порошок полностью суспендирован. В противном случае
повторите умеренное встряхивание в течение еще 30 секунд.
 Этап 6.
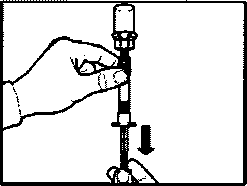
Этап 6.
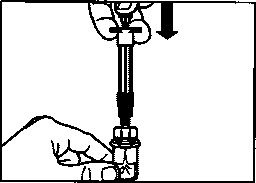
• Переверните флакон со шприцем вверх дном и медленно вытяните поршень назад, чтобы все содержимое флакона переместилось из флакона в шприц.
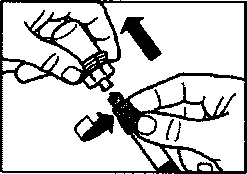
• Отвинтите шприц от адаптера для флакона.
 Этап 7.
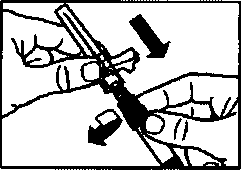
Этап 7.
• Привинтите безопасную инъекционную иглу на шприц.
• Снимите защитный колпачок с иглы.
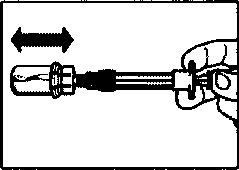
• Для предотвращения возникновения осадка можно слегка встряхнуть шприц до получения однородной молочной суспензии.
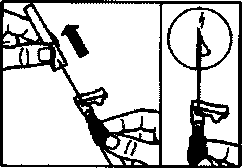
• Слегка постучите по шприцу для удаления видимых пузырьков и выдавите их из шприца.
• Суспензия Сандостатин ЛАР готова. Следует
немедленно выполнить инъекцию.
 Этап 8
Этап 8
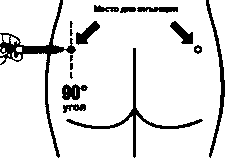
• Сандостатин ЛАР предназначен только для глубокой внутримышечной инъекции в ягодичную область. Категорически
НЕДОПУСТИМО ВНУТРИВЕННОЕ введение.
• Обработайте место инъекции спиртовым тампоном.
• Полностью введите иглу в левую или в правую ягодицу под прямым углом к коже.
• Немного потяните поршень назад, чтобы убедиться, что иглой не повреждены кровеносные сосуды. В случае повреждения кровеносного сосуда следует изменить место для инъекции.
• Медленно нажимайте на поршень до полного опорожнения шприца. Извлеките иглу из места инъекции и установите защитный колпачок (как показано на рисунке этапа 9).
 Этап 9
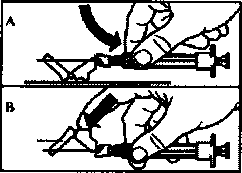
Этап 9
• Установите защитный колпачок на иглу одним из двух способов:
- либо прижмите подвижную секцию защитного колпачка к твердой поверхности (рисунок А).
- либо надавите вперед на шарнир защитного колпачка указательным пальцем (рисунок В).
• Должен раздаться щелчок, который подтверждает правильную установку защитного колпачка.
• Сразу же выбросьте шприц в контейнер для острых предметов.

 • Комплект Сандостатин ЛАР следует достать из холодильника.
• Комплект Сандостатин ЛАР следует достать из холодильника. Этап 2.
Этап 2. • Удерживая упаковку адаптера для флакона, поместите адаптер для флакона на верхнюю часть флакона и нажмите на него до упора так, чтобы он встал на место, при этом должен раздаться щелчок.
• Удерживая упаковку адаптера для флакона, поместите адаптер для флакона на верхнюю часть флакона и нажмите на него до упора так, чтобы он встал на место, при этом должен раздаться щелчок. • Снимите вертикальным движением упаковку с адаптера для флакона.
• Снимите вертикальным движением упаковку с адаптера для флакона. Этап 3.
Этап 3. • Медленно нажимая вниз на поршень, введите весь растворитель во флакон.
• Медленно нажимая вниз на поршень, введите весь растворитель во флакон. Этап 4.
Этап 4. Этап 5.
Этап 5. Этап 6.
Этап 6. • Отвинтите шприц от адаптера для флакона.
• Отвинтите шприц от адаптера для флакона. Этап 7.
Этап 7. • Слегка постучите по шприцу для удаления видимых пузырьков и выдавите их из шприца.
• Слегка постучите по шприцу для удаления видимых пузырьков и выдавите их из шприца. Этап 8
Этап 8 Этап 9
Этап 9